Úvod
Naša koža je domovom miliónov baktérií, húb a vírusov, ktoré tvoria mikrobióm našej kože. Podobne ako v našom črevnom systéme, hrajú kožné mikroorganizmy podstatnú úlohu pri ochrane voči napadnutiu patogénmi, pri zlepšovaní nášho imunitného systému a rozpadu prírodných produktov. Koža je považovaná za najväčší orgán ľudského tela, je kolonizovaná prospešnými mikroorganizmami a slúži ako fyzická bariéra voči invázii patogénov. V prípadoch, keď je bariéra porušená alebo keď je narušená rovnováha medzi komenzálmi a patogénmi, môže dôjsť k ochoreniam kože alebo dokonca k systémovým ochoreniam. Lokality ľudskej kože možno kategorizovať podľa ich fyziologických vlastností na:
- Mazové (mastné)
- Vlhké
- Suché
Štúdium zloženia mikrocenózy na rôznych miestach má nesmiernu cenu pri objasňovaní etiológie bežných kožných ochorení, ktoré často prednostne postihujú špecifické miesta pokožky, ako je ekzém lakťa alebo psoriáza na vonkajšej strane lakťa.
Rozdiely v detekcii mikroorgnizmov
Tradične sa skúmali kožné mikrobiálne komunity pomocou metód založených na živých kultúrach. Tento prístup selektuje mikroorganizmy, ktorým sa darí rásť v umelých podmienkach inkubátorov. Podceňila sa tak celková rozmanitosť mikrobiálnej komunity, pretože nie všetky mikroorganizmy sú kultivovateľné. Napríklad, kožné baktérie z rodu Staphylococcus sa kultivujú ľahšie ako Propionibacterium spp. alebo Corynebacterium spp. Preto je potrebné obísť tento zastaralý postup a zachytiť úplnú rozmanitosť kožného mikrobiómu. Preto výskumníci začali používať sekvenčné metódy založené iba na genetike. Pôvodné sekvenčné prístupy využívali variácie sekvencií v konzervovaných taxonomických markeroch ako molekulárne odtlačky prstov pri identifikácii jednotlivých členov mikrobiálnych spoločenstiev. Pre baktérie sa používa 16S ribozomálna RNA (rRNA), zatiaľ čo pre huby je výhodná vnútorná transkribovaná spacer 1 (ITS1) oblasť eukaryotického ribozomálneho génu.
Genetické sekvenovanie
Vzhľadom na to, že sekvenčné technológie pokročili od sekvencovania Sanger po 454 pyrosekvenciu a potom sekvenovanie Illumina, bol tento pôvodný prístup pravidelne prispôsobovaný tak, aby vyhovoval zvyšujúcej sa hĺbke čítania a kratším dĺžkam čítania. To sa dosiahlo s novými primérmi pre kratšie amplikóny (zmožené genetické úseky), clusterovými metódami na prekonanie sekvenčnej chyby a metódami zostavovania, aby sa spojili spárované dáta. Pri kratších dĺžkach amplikónu (~300 bp v porovnaní s > 1000 bp pri sekvenovaní Sanger), môže byť analyzovaný len subregión génu 16S rRNA. Tento postup si vyžaduje optimalizované priméry, ktoré sa viažu na špecifické oblasti 16S rRNA génu na zachytenie genetickej diverzity bakteriálnej populácie. Primérové páry, ktoré sa používajú pri kožných mikrobiálnych štúdiách, by mali byť optimalizované tak, aby zosilnili a rozlíšili prevládajúce kožné mikrobiálne taxóny. Obidve metódy využívajú prístup založený na čítaní sekvencie, v ktorom sú sekvencie porovnávané s referenčnými databázami na klasifikáciu mikroorganizmov na úrovni rodu a ak je to možné tak aj na druhovej úrovni.
Väčšina výskumov mikrobiálnej komunity pokožky využila sekvenovanie amplikónov. V priebehu niekoľkých posledných rokov však významné technické a analytické objavy umožnili štúdium metagenomiky. Obrázok 1 ukazuje technické a procedurálne rozdiely medzi metódov amplikónov a metagenomikou.
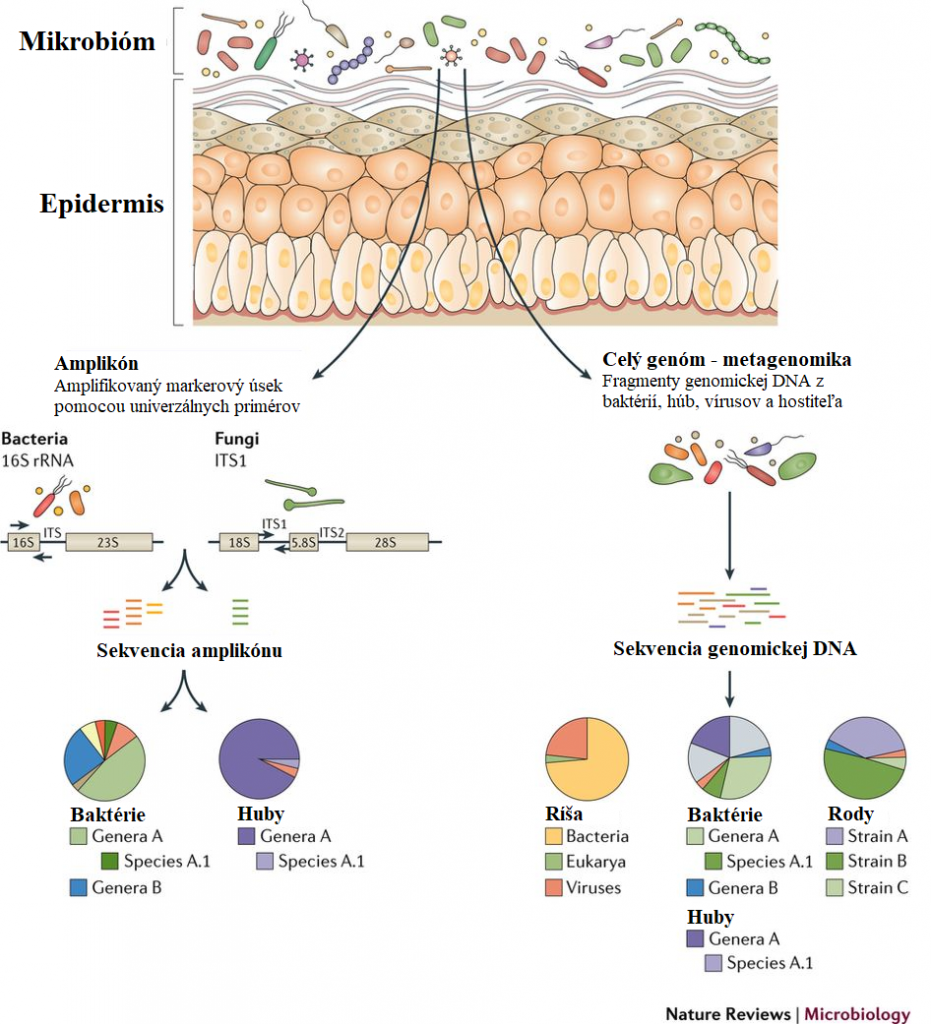
Metagenomická analýza
Metagenomiká analýza nezachytáva sekvencie špecifických cieľových oblastí ako amplikónová ale súčasne zachytáva všetok genetický materiál vo vzorke, vrátane ľudskej, bakteriálnej, hubovej, archeálnej a vírusovej DNA. Ďalšou výhodou metagenomického sekvenovania je to, že tieto dátové súbory poskytujú dostatočné rozlíšenie na odlíšenie druhov a dokonca aj kmeňov v rámci jedného druhu. Presne to je kľúčové pri identifikácii členov rodu Staphylococcus, ktoré sa ťažko klasifikujú na druhovú úroveň pri väčšine prístupov sekvenovania amplikónov. Schopnosť diferencovať mikroorganizmy až na úroveň kmeňa je dôležitá, pretože takéto štúdie dokážu viac odhaliť funkčné rozdiely medzi skúmanými druhmi.
Kožný mikrobióm a zdravie
Pred tým, než začneme robiť závery pred vyšetrením zmien v mikrocenóze, ktoré sú spojené s chorobnými stavmi, musia vedci najprv stanoviť základnú líniu a normálnu zmenu v mikrocenóze zdravých jedincov.
Zloženie zdravej mikroflóry kože
So sekvenčných prieskumov zdravých dospelých jedincov bolo zistené, že zloženie mikrobiálnych spoločenstiev je primárne závislé od fyziológie miesta na koži. Mazové miesta na koži obýva viac lipofilných druhov rodu Propionibacterium, zatiaľ čo baktérie, ktorým sa darí vo vlhkom prostredí, ako je napríklad Staphylococcus a Corynebacterium, sa prednostne vyskytujú na vlhkých miestach, vrátane ohybu kolien a nôh.
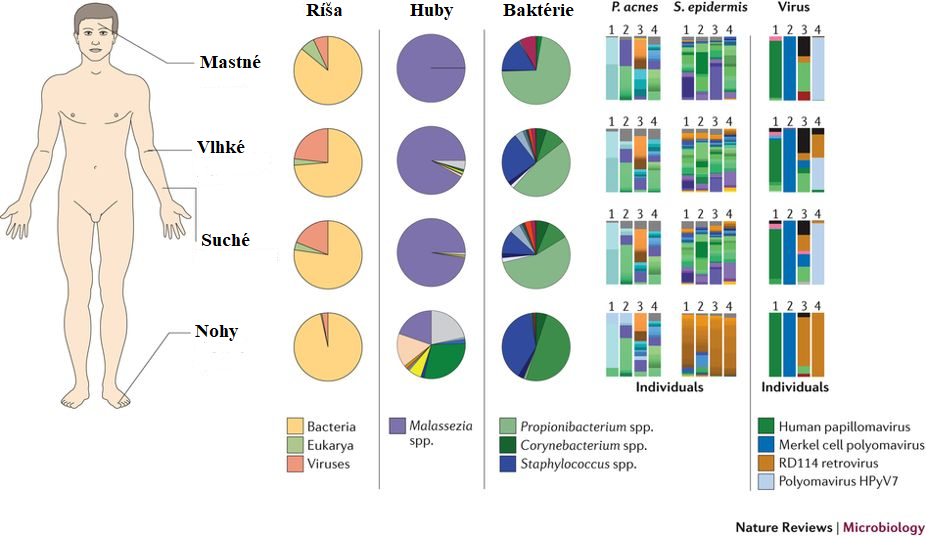
Na rozdiel od bakteriálnych spoločenstiev, zloženie komunity húb bolo podobné naprieč všetkými miestami na tele bez ohľadu na fyziológiu. Huby rodu Malassezia prevládajú na hlavných miestach tela a paží, zatiaľ čo miesta na nohách boli kolonizované rôznorodejšou kombináciou Malassezia spp., Aspergillus spp., Cryptococcus spp., Rhodotorula spp., Epicoccum spp. a ďalších (obrázok 2). Baktérie boli najpočetnejšou skupinou naprieč miestami na koži a huby naopak v najmenšom zastúpení (obrázok 2). Je treba podotknúť, že existuje však oveľa viac baktérií ako húb, ktoré čiastočne prispeli k tomuto pozorovanému rozdielu. Zaujímavosťou je, že celková hojnosť húb bola nízka, dokonca aj na nohách, kde bola naopak diverzita húb vysoká.
Na rozdiel od baktérií a húb, kolonizácia DNA eukaryotickými vírusmi bola špecifická individuálne než pre anatomické miesto (obrázok 2). Okrem bakteriofágov (vírusy baktérií) môžu zohrávať eukaryotické vírusy tiež úlohu pri kožných ochoreniach, ako to zdôrazňuje objavenie polyomavírusu buniek Merkel, onkovírus, ktorý spôsobuje vzácnu, ale agresívnu formu rakoviny kože.
Stabilita mikrobiómu
Použitím pozdĺžneho odberu vzoriek sa zistilo, že kožné mikrobiálne komunity boli počas dvojročnej štúdie prevažne stabilné napriek neustálim zmenám životného prostredia. Na základe analýz na úrovni kmeňov a nukleotidov bola táto stabilita určená udržiavaním kmeňov v priebehu času, a nie reakciou bežných druhov z prostredia. Podobne v longitudinálnom prieskume črevného traktu sa zistilo, že špecifické druhy mikroflóry jednotlivca pretrvávajú na jeden alebo viac rokov. Bakteriálne a hubové spoločenstvá na mazových miestach boli najstabilnejšie. Mikrobiálne komunity nôh boli najmenej stabilné a DNA eukaryotické vírusy sa menili najčastejšie. Relatívna nestabilita mikrobiálnych spoločenstiev môže byť spôsobená prechodnou prítomnosťou húb v prostredí.
Rôzne miesta na koži
Okrem úrovne druhov poskytujú metagenomické dáta dostatočné rozlíšenie na preskúmanie rozmanitosti druhov dominantných kožných baktérií. V porovnaní s črevnou komunitou má koža nízku mikrobiálnu biomasu, ktorá vedie k vysokým počtom sekvencií hostiteľa a nízkym mikrobiálnym sekvenciám v metagenomických vzorkách. Napriek nízkej úrovne čítania je možná identifikácia najrozšírenejších druhov kože, pretože existujú zbierky sekvenovaných referenčných genómov. V rôznych miestach tela sa zistilo, že jedinci sú kolonizovaní rôznymi multifyletickými spoločenstvami kmeňov baktérií Propionibacterium acnes a Staphylococcus epidermidis (obrázok 2). Okrem toho kmene baktérie S. epidermidis z komenzálneho kmeňa demonštrovali špecifickosť miesta s tropizmom pre ľudské nohy. Popisovanie spoločenstiev v rozlíšení na úrovni kmeňa sú preto dôležité. Rozdiely v obsahu génov medzi druhmi a v rámci druhu môžu určiť funkčné rozdiely medzi zdravím a chorobou. Napríklad antibiotická rezistencia a gény virulencie sú variabilne prítomné v kmeňoch baktérií P. acnes a S. epidermidis. Analýza kmeňových spoločenstiev iných mikrobiálnych druhov kože bude vyžadovať vytvorenie ďalších komplexných referenčných genómových knižníc ale aj vývoj nových výpočtových nástrojov, ktoré budú schopné klasifikovať kmene z metagenomických údajov s nízkym pokrytím. V súčasnej dobe je rozlíšenie na úrovni kmeňa bez mapovania na referenčné genómy obmedzené na jedno-molekulárne, dlho čitateľné metagenomické sekvenčné štúdie. Budúce funkčné štúdie umožnia výskumníkom objasniť, či niektoré kmene poskytujú odolnosť voči kolonizácii, voči iným kmeňom rovnakého alebo odlišného druhu ako dôležitý krok vo vývoji prebiotických a probiotických stratégií.
Živiny pre mikroorganizmy
V porovnaní s bohatším prostredím našich čriev, koža neobsahuje veľa živín nad rámec základných proteínov a lipidov. Ak chcú mikroorganizmy prežiť v tomto chladnom, kyslom a suchom prostredí (Box 1), domovská mikroflóra našej kože sa prispôsobila, aby využívala zdroje, ktoré sú prítomné v pote, maze a rohovine (tabuľka 1). Napríklad fakultatívny anaerób P. acnes je schopný prosperovať v anoxickej mazovej žľaze a pomocou proteáz uvoľnuje arginín (aminokyselinu) z kožných proteínov. Lipázy používa na degradáciu triglyceridových lipidov v maze, čím uvoľňuje voľné mastné kyseliny, ktoré podporujú priľnavosť baktérií. U vzoriek z tváre sa preukázalo, že hladiny mazu na líci pozitívne korelujú s početnosťou baktérií rodu Propionibacterium spp. Zaujímavé je, že u cicavcov, ako sú myši, potkany a psy, ktoré produkujú menšie množstvá mazu bohaté na triglyceridy, P. acnes rastie slabšie, a preto sa vyskytuje pri nižších počtoch.
Genetická výbava
Lipidy mazu a odumreté bunky kože sú rovnako využívané auxotrofickými druhmi rodu Malassezia a Corynebacterium, pretože nie sú schopné produkovať svoje vlastné lipidy. Corynebacterium spp. využívajú tieto lipidové zlúčeniny na vytvorenie korymylových kyselín, ktorými obkolesujú svoj povrch buniek. V súlade s nedostatkom uhľovodíkov v kožnom prostredí bohatom na lipidy, Malassezia spp. nesie genetický kód obsahujúci lipázové gény a gény pre enzýmy využívajúce sacharidy v porovnaní s genetickým materiálom iných sekvenovaných húb je minimálny. Takéto rozdiely môžu vysvetľovať, ako dokážu druhy rodu Malassezia prevažívať na koži dospelých jedincov. Baktérie rodu Staphylococcus spp. si vyvinuli mnohé stratégie na prežitie na koži, vrátane ich schopnosti byť halotolerantnými (to znamená, aby odolali vysokému obsahu soli v pote) a dokázali využiť močovinu, ktorá je prítomná v pote a využívajú ju ako zdroj dusíka. Aby sa ďalej podporila ich kolonizácia, rôzne druhy rodu Staphylococcus spp. produkujú adherény, ktoré podporujú prichytenie k pokožke a proteázy, ktoré uvoľňujú živiny z odumretých buniek kože. Celkovo nesie pokožka heterogénnu komunitu mikroorganizmov, z ktorých má každý odlišné prispôsobenie sa prostrediu, aby na koži dokázali prežiť.
Ekológia mikrobiálneho spoločenstva kože
U dospelích jedincov sa udržiava stabilné zloženie kožných mikrobiálnych spoločenstiev. Výskumy trvali najmenej 2 roky, avšak príčiny, ktoré formujú a udržiavajú takéto zložité komunity mikroorganizmov, zostávajú zatiaľ nepochopené.
Počiatočná kolonizácia kože a jej zmeny
U novorodencov je počiatočná kolonizácia kože závislá od spôsobu pôrodu. Novorodenci narodení vaginálne získavajú baktérie, ktoré kolonizujú vagínu, zatiaľ čo novorodenci narodení cisárskym rezom sú kolonizovaný mikroorganizmami, ktoré sa s kožou spájajú u dospelých. Dlhodobé účinky týchto počiatočných spôsobov kolonizácie kože u novorodencov zostávajú neznáme a na riešenie tejto nedoriešenej otázky je potrebné vykonať metagenomické sekvenovanie až na úrovni kmeňov.
V črevnom trakte sa mikrobiálne spoločenstvá stabilizujú v priebehu 3 rokov. Pred touto stabilizáciou sú kmene mikroorganizmov pravdepodobne prenášané z tesných kontaktov a členov rodiny. Predpokladá sa, že následne sa udržiavajú po celý život. Na rozdiel od tohto je relatívna abundancia kožných mikrobiálnych druhov reštrukturalizovaná počas puberty, v čase, keď zvýšené hladiny hormónov stimulujú mazové žľazy a produkujú nadbytočné množstvá kožného mazu. Takže koža postpubescentných jedincov podporuje expanziu lipofilných mikroorganizmov, ako sú baktérie rodu Propionibacterium spp., Corynebacterium spp. a huby rodu Malassezia spp. Naopak, predpubertálne deti majú na koži vyšší výskyt baktérií Firmicutes (Streptococcaceae spp.), Bacteroidetes a Proteobacteria (betaproteobaktérie a gammaproteobaktérie) a rôznorodejšiu komunitu húb. Zostáva však nejasné, či sa počas puberty získavajú nové kmene alebo či sa mení iba relatívna abundancia existujúcich kmeňov. Celkovo sú tieto zmeny v mikrobióme kože súvisiace s vekom zaujímavé, keďže veľa kožných porúch je spojených práve s vekom. Napríklad prípady atopickej dermatitídy súvisiacej s rodom Staphylococcus klesajú u väčšiny detí pred pubertou, zatiaľ čo Malassezia hubou asociovaná tinea versicolor je bežnejšia u dospelých ako detí. Avšak, sú potrebné ďalšie výskumy aby sa charakterizovali kožné mikrobiálne faktory u starších jedincov ako aj fyziológia a predispozície na kožné infekcie.
Interakcie medzi kožnými mikrobiálnymi druhmi
Zhromažďovanie, stabilita a funkcia mikrobiálnej komunity sa riadi hostiteľskými faktormi, ako aj interakciami medzi týmito mikroorganizmami. Mikroorganizmy môžu pôsobiť konkurenčne, aby sa navzájom vylúčili alebo synergicky, aby sa vzájomne podporovali. Staphylococcus aureus ako častá kožná baktéria sa stala centrom mnohých kolonizačných štúdií. S. aureus kolonizuje nosné dutiny minimálne jednej tretiny populácie a jej prítomnosť je významným rizikovým faktorom pri potenciálnych infekciách. Pri klinických testoch sa ukázalo, že za infekcie krvného riečišťa zodpovedá približne 80% izolátovS. aureus, ktoré boli identifikované v nosných dutinách jednotlivcov. Eradikácia S. aureus z nosných dutín pacientov podstatne znižuje ich náchylnosť k invazívnym infekciám.
Staphylococci v súboji
Vzhľadom na to, že S. aureus si často vyvíja rezistenciu voči antibiotikám a vývoj vakcín vykazuje obmedzenú účinnosť, je alternatívnou stratégiou eradikácie použitie komenzálnych mikroorganizmov. Tento spôsob je však aktívnou oblasťou výskumu. Podobné konkurenčné štúdie skúmali, ako mikroorganizmy v pôde medzi sebou súťažia prostredníctvom produkcie antibiotík. Prvé mikroorganizmy, o ktorých sa uvádza, že inhibujú tvorbu biofilmu S. aureus, je podskupina kmeňa S. epidermidis. Neskôr sa zistilo, že S. epidermidis a jeho kmene degradujú proteíny, ktoré sú rozhodujúce pre tvorbu biofilmu S. aureus a adhéziu na epitel hostiteľa. Keď sa proteázová aktivita skombinovala s antimikrobiálnymi aktivitami ß-defenzínu, výsledná baktericídna aktivita bola dostatočná na usmrtenie S. aureus v biofilmoch (obrázok 3). Je zaujímavé, že drvivá väčšina sekvenovaných S. epidermidis izolátov obsahuje gén esp (gseA), avšak v doterajších štúdiách iba malá podskupina naozaj exprimovala gén gseA. Tento fakt je dôležitou pripomienkou, že vlastníctvo génu ešte nezaručuje jeho funkčnosť a exprimovanie.
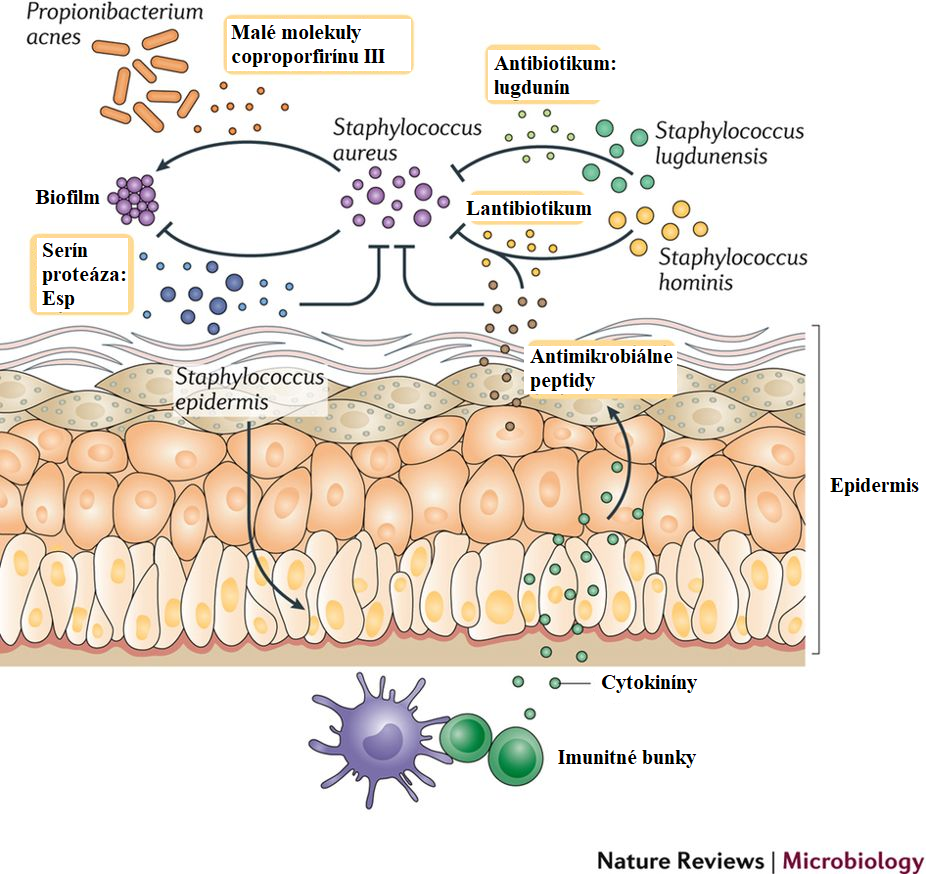
V najnovšej štúdii Staphylococcus lugdunensis inhiboval rast S. aureus produkciou antibiotického lugdunínu, nového cyklického peptidu obsahujúceho tiazolidín (obrázok 3). Toto zistenie je dôležité pre dlhodobý terapeutický potenciál, pretože ani po niekoľkých generáciách S. aureus si nikdy nevyvinul rezistenciu voči antimikrobiálnym účinkom lugdunínu. Nedostatok rezistencie je v ostrom kontraste s tradičnými antibiotikami, voči ktorým si organizmy vyvíjajú rezistenciu, a zdôrazňuje, že prirodzene odvodené látky môžu byť účinnejším prostriedkom pri potláčaní oportunistických patogénov.
V jednej zo štúdii sa preukázalo, že viaceré koaguláza negatívne druhy rodu Staphylococcus spp., S. epidermidis a S. hominis produkujú nové lantibiotiká, ktoré sú schopné synergizovať s humánnym kateicidínovým antimikrobiálnym peptidom LL-37 a inhibovať rast S. aureus. Kmene produkujúce tieto lantibiotiká sa nevyskytovali u jedincov s atopickou dermatitídou, ktorí sú často kolonizovaní S. aureus. Okrem toho lokálna aplikácia týchto kmeňov produkujúcich antimikrobiálne látky znížila kolonizáciu S. aureus len u malého počtu jedincov s atopickou dermatitídou, čo dokazuje translačný potenciál probiotickej stratégie.
Staphylococci vs. iné baktérie
Nie všetky mikroorganizmy však inhibujú S. aureus. Skôr sa zistilo, že niektoré druhy rodu Propionibacterium by mohli indukovať agregáciu S. aureus a tvorbu biofilmu spôsobom závislým od dávky, rastovej fázy a pH (obrázok 3). V samostatnej in vitro štúdii sa zistilo, že S. aureus sa mení z virulentného na komenzála, ak je vystavený komenzálnemu druhu Corynebacterium striatum. Táto schopnosť zmeniť správanie S. aureus otvára terapeutickú možnosť modulácie jeho správania namiesto zničenia samotného patogéna.
Iné druhy
Existujú tiež príklady interakcií medzi inými kožnými mikroorganizmami. Corynebacterium accolens modifikuje lokálne prostredie kože a inhibuje tak rast oportunistického patogéna Streptococcus pneumoniae. Táto odpoveď bola závislá od C. accolen, ktorý použitím lipázovej aktivity LipS1 uvoľnuje antibakteriálne voľné mastné kyseliny z triacylglycerolov na povrchu kože. V inej štúdii sa vykonali párové antagonistické testy s izolátmi zo zbierkových kmeňov S. epidermidis a P. acnes. Jeden kmeň P. acnes (I-2) vykazoval selektívne vyššiu antimikrobiálnu aktivitu voči S. epidermidis ako iné P. acnes kmene. Pravdepodobne to bolo v dôsledku tiopeptidu konzervovaného naprieč kmeňmi typu I-2. Naopak, väčšina testovaných kmeňov S. epidermidis bola schopná inhibovať rast P. acnes v in vitro podmienkach. Autori tejto štúdie vypočítali rôzne mobilné genetické prvky, ktoré by mohli byť zodpovedné za tento fenotypový prejav v rôznych kmeňoch.
Na rozdiel od mnohých interakcií medzi druhmi sú výskumy dynamiky medzi kmeňmi v rámci druhu zriedkavejšie. Extrapolácie z metagenomických údajov odhalili dva spôsoby kolonizácie ľudského črevného traktu. Pre niektoré druhy existuje jediný dominantný kmeň, zatiaľ čo pre iné druhy existujú viaceré kmene na podobných úrovniach.
Na koži, P. acnes a S. epidermidis existujú ako stabilné heterogénne komunity jednotlivých kmeňov. Štúdie ukázali, že vo vnútri črevného traktu spoločenstvo druhov rodu Clostridium môže pôsobiť synergicky na zvýšenie regulačných odpovedí T buniek vo väčšom rozsahu, než akýkoľvek jednotlivý druh môže spôsobiť samotne. Pri koži sú potrebné podobné štúdie aby sa preukázali možné funkčné výhody heterogénnych kmeňových spoločenstiev.
Kožný mikrobióm pri ochorení
Interakcie medzi druhmi mikroflóry formujú rezidentnú mikrobiálnu komunitu a zabraňujú kolonizácii patogénnym baktériam v procese označovanom ako „kolonizačný odpor“ alebo “kolonizačná rezistencia”. Avšak v určitých situáciach sa baktérie, ktoré sú bežne prospešné pre ich hostiteľov, môžu stať patogénnymi. Veľa bežných kožných ochorení je spojená so zmenami v mikroflóre a nazýva sa dysbióza. Takáto dysbióza je často spôsobená spoločnými komenzálnymi druhmi. Očakáva sa, že vzácne aj bežné kožné ochorenia majú svoju podstatu v jednotlivých druhoch ale aj v zmenách mikrobiálnej komunity. Ďalšie longitudinálne klinické štúdie môžu objasniť mechanické prepojenie medzi druhmi húb a lupinami, infekciami nôh alebo medzi vírusmi a bradavicami.
Mikroorganizmy spojené s bežným akné
Akné je prevládajúca choroba u dospievajúcich (acne vulgaris). Je to chronický zápalový stav kože, ktorý je spájaný s baktériouP. acnes, najhojnejším mikroorganizmom v mikrobióme zdravých dospelých jedincov. Na funkčnej úrovni sú profily génovej expresieP. acnes odlišné medzi jednotlivcami s akné a jednotlivcami bez akné. Pozorovanie, že takmer všetci dospelí sú kolonizovaní sP. acnes ale len menšina z nich má akné zdôrazňuje význam štúdia ochorenia v širšom kontexte hostiteľskej genetiky, imunitných alebo bariérových defektov, mikrobiómu a životného prostredia. Napríklad, zvýšená sekrécia kožného mazu je spojená s patofyziológiou akné, pretože miera sekrécie koreluje so závažnosťou klinických príznakov. V štúdii používajúcej fluorescenčnú mikroskopiu na vizualizáciu P. acnes vo folikuloch vzoriek kožnej biopsie bol vývoj akné v podstate spojený s prítomnosťou P. acnes vo folikuloch a tvorbou biofilmov.
Historicky je doplnok vitamínu B12 spojený s akné. V poslednej dobe súvisí akné s doplnkovým vitamínom B12, ktorý potláča biosyntézu vitamínu B12 u P. acnes, čo následne vedie k zvýšeniu produkcie porfyrínov a tie môžu vyvolať zápal pokožky a rozvoj akné. Zaujímavé je, že akné asociované kmenmi P. acnes produkujú podstatne vyššie hladiny porfyrínov.
Staphylococcus aureus a atopická dermatitída
Atopická dermatitída (tiež známa ako ekzém) je chronické, recidivujúce zápalové ochorenie s viacerými faktormi, ktoré prispievajú k poškodeniu epidermálnej bariéry, aktivácii imunitných buniek a zmenám v spoločenstve súvisiacich mikroorganizmov kože. Citlivosť na atopickú dermatitídu bola spojená s mutáciami vo viac ako 30 hostiteľských génových miestach vrátane génu kódujúceho proteín kožnej bariéry filagrín a génov spojených s imunitným systémom. OkremS. aureus , ktorý sa bežne vyskytuje na koži jedincov s atopickou dermatitídou, existujú ďalšie faktory, ktoré podporujú hypotézu, že mikroflóra má vplyv na patogenézu chorôb. Atopická dermatitída je klinicky liečená zmäkčovadlami, ktoré podporujú integritu bariéry a imunosupresívnymi liekmi, ako sú steroidy. V prípadoch, keď dôjde k infekcii alebo pretrvávaniu ochorenia, môžu sa použiť antimikrobiálne prístupy (napríklad antibiotiká a zriedené bieliace činidlá) a ich úspech sa preukázal v súvislosti s poklesom relatívnej abundancie S. aureus. Ich celková účinnosť je však neistá.
Abundancia Stapylococcus
V longitudinálnych štúdiách pediatrických jedincov s atopickou dermatitídou 16S rRNA a sekvenovanie celých genómov klinických vzoriek ukázalo, že relatívna abundancia Staphylococcus spp., najmä S. aureus a S. epidermidis , vzrástla pri vypuknutí ochorenia (epizodická exacerbácia) oproti stavu po a že relatívna abundancia stafylokokov korelovala so závažnejším stavom choroby pri vypuknutí ochorenia. Na úrovni kmeňa sa zistilo, že jedinci s atopickou dermatitídou sú kolonizovaní heterogénnejšími spoločenstvami S. epidermidis a tí s ťažším ochorením boli kolonizovaní dominantne kmeňmi S. aureus. Korelácia S. aureus s atopickou dermatitídou počas aktívnej exacerbácie ochorenia je dobre zdokumentovaná. Avšak funkčná úloha stafylokokov pri zvládaní ochorenia atopickej dermatitídy je zle pochopená. Je potrebný pozdĺžny odber vzoriek v častejších intervaloch ešte predtým, ako je potrebné zistiť, či zvýšené hladiny stafylokokov predchádzajú klinickým príznakom, čo by podporilo teóriu, že stafylokoky v dôsledku toho prispievajú k počiatočnému nástupu zápalu, a nie k jeho rozvynutiu. To si vyžaduje ďalšie skúmanie, keďže v predbežných štúdiách sa zistil väčší počet Staphylococcus spp. v dvoch mesiacoch u dojčiat, u ktorých nedošlo k rozvoju atopickej dermatitídy o 1 rok, ako u tých, u ktorích sa vyvinula atopická dermatitída vo veku 1 roka. Expozícia Staphylococcus spp. v ranom veku je užitočná pre správne nasmerovanie imunitného systému.
pH a atopická dermatitída
Ďalšia štúdia zameraná na genómové sekvenovanie porovnávala kožu dospelých s atopickou dermatitídou s kontrolnou kohortou a identifikovala zvýšené počty rodov Streptococcus spp. a Gemella spp. a nižšie počty rodu Dermacoccus spp. u jedincov náchylných voči atopickej dermatitíde. Na funkčnej úrovni, štúdie ukázali, že mikrobióm týchto jedincov je prispôsobený tak, aby generoval prebytok amoniaku. Ten vysvetľuje vysoké hodnoty pH, ktoré sa pozorujú pri atopickej dermatitíde.
Biodiverzita pri ataopickej dermatitíde
Znížená rozmanitosť kožného mikrobiómu u jedincov s atopickou dermatitídou súvisí so znížením biodiverzity životného prostredia v oblastiach okolo ich domovov. V jednej štúdii obsahovala koža zdravých jedincov väčšiu rozmanitosť gammaproteobaktérií, ktorých prítomnosť korelovala s vyššou expresiou IL-10 v krvi. Následne, štúdia za použitia in vitro a in vivo experimentov na zvieratách ukázala, že gammaproteobacteria rodu Acinetobacter by mohla vyvolať silnú T-helper 1 (TH1) a protizápalovú imunitnú odozvu. V štúdii, ktorá skúmala mikrobióm pokožky jedincov s ichtyózou vulgaris a deficitom filaggrínu, došlo k nedostatočnej reprezentácii grampozitívnych anaeróbnych kokov v porovnaní s ich prítomnosťou v zdravých kontrolách, čo naznačuje, že defektné odumreté bunky kože sú dostatočné na zmenu kožného mikrobiómu a môžu viesť k dysbióze, ktorá je spojená s ekzémom.
Toxíny S. aureus a imunita
Vzhľadom na asociáciu S. aureus s atopickou dermatitídou a inými kožnými ochoreniami a infekciami krvného obehu sa mnohé štúdie zamerali na interakcie medzi S. aureus, jeho toxínmi a imunitným systémom. Napríklad S. aureus δ-toxín indukuje degranuláciu mastocytov (žírnych buniek), ktorá podporuje vrodenú aj adaptačnú imunitnú odpoveď druhého typu. α-toxín S. aureus môže tiež indukovať produkciu imunoglubulínov. Ak vystavili vedci bunkové komponenty S. aureus T bunkám, tak ani neproliferovali ani nevyrábali cytokíny, čo naznačuje, že produkty S. aureus môžu aktivovať imunitný systém a dočasne ho paralyzovať. Okrem zacielenia sa na imunitné bunky sa ukázalo, že S. aureus spúšťa adipocyty tak, aby rýchlo proliferovali a produkovali zvýšené hladiny antimikrobiálneho peptidu katelicidínu ako obranného mechanizmu hostiteľa. Tieto príklady demonštrujú mnohé spôsoby, ako S. aureus iniciuje alebo exacerbuje kožné poruchy v širšom kontexte bariérových defektov alebo zmenenej imunity. V skutočnosti sa preukázalo, že v kontexte bariérových defektov S. aureus je schopný prestupovať epidermis do dermis, kde narazí na imunitné bunky a spúšťa expresiu zápalových cytokínov IL-4, IL-13 a IL-22 a tymického stromálneho lymfopoetínu. Schopnosť S. aureus spúšťať kožnú imunitnú odpoveď môže byť závislá od kmeňa, čo zdôrazňuje význam hodnotenia fenotypu naprieč izolátmi druhu. Hoci mnohé z týchto experimentov boli vykonané na myších modeloch, sú relevantné aj pre ľudí, pretože mnohé z dráh, ktoré sú základom zápalu a imunity v myšacej koži, sa javia ako dôležité pri infekciách a chorobách aj u ľudí.
Experimenty u myší
Aj keď bol preukázaný zápalový potenciál S. aureus a dysbióza je bežná u mnohých ochorení kože, stále nie je známe, či sú tieto zmeny dôsledkom chorobného stavu alebo či S. aureus prispieva k vzniku tohto ochorenia. Experimenty s myšacími modelmi, ktoré sú geneticky a fyzicky postihnuté v produkcii kožnej bariéry alebo imunologických defektov, sa použili na určenie prínosu mikroflóry k ochoreniu kože. Zmeny v kožných mikrobiálnych spoločenstvách, charakterizované nadmerným rozmnožovaním Corynebacterium mastitidis , Corynebacterium bovis a S. aureus predchádzali vývojovým znakom atopickej dermatitídy. Cielené antibiotické liečenie týchto zvierat bolo dostatočné na zvrátenie dysbiózy a elimináciu zápalu kože, čo dokazuje príčinnú súvislosť medzi zmenami bariéry kože, dermatitídou a mikrobiómom.
Kožný mikrobióm jedincov s primárnou imunodeficienciou
Zatiaľ čo sa niekoľko štúdií zaoberalo témou, ako mikroorganizmy posilňujú náš imunitný systém, štúdium jedincov s primárnou imunodeficienciou (PID) poskytuje príležitosť porozumieť úlohe imunity pri určovaní štruktúry mikrobiálnych spoločenstiev. Základom zdôvodnenia týchto vyšetrení sú bežné kožné prejavy jedincov s PID, najmä ekzémom. Na tento účel boli odobraté vzorky kožných mikroflór od jedincov so zriedkavými monogénnymi PID, syndrómom hyper IgG, Wiskott-Aldrichovým syndrómom a dedikátorom syndrómu cytokinézy 8. Napriek odlišným základným mutáciám sú všetky choroby charakterizované ekzémom ako podobné kožné ochorenie, zníženie množstva T a B buniek, premenlivá eozinofília a zvýšené hladiny IgE. Aj keď existuje celková podobnosť druhov baktérií, ktoré kolonizujú pokožku zdravých jedincov, koža jedincov s PID je ekologicky s menšou časovou stabilitou. Napriek tomu, že osoby s PID sú kolonizované s oportúnistickými hubami (napríklad Candida spp., alebo Aspergillus spp.), baktériami (napríklad Serratia marcescens), ktoré zvyčajne v kontrolách chýbajú, tieto mikroorganizmy stále patria do skupiny, ktoré sa bežne vyskytujú na koži. To naznačuje, že mikroorganizmy mimo týchto primárnych skupín nie sú schopné stabilne prežiť v prostrediach s nedostatkom živín na koži. V samostatnej štúdii jedincov s PID spôsobených mutáciami v signálovom prevodníku a aktivátorom transkripcie 1 (STAT1) alebo STAT3 bola koža kolonizovaná viacerými gramnegatívnymi baktériami, najmä rodom Acinetobacter spp. Rovnako došlo k zníženiu počtu baktérií rodu Corynebacterium spp. v porovnaní s hladinami u zdravých kontrol. Na identifikáciu možných zmien vo vírusových spoločenstvách je potrebné vykonať metagenomické sekvenovanie vzoriek u týchto jedincov, pretože niektorí pacienti s PID často trpia vírusovými kožnými infekciami.
Mikroorganizmy pri chronických infekciách rán
Okrem klasických kožných ochorení bolo tiež dokázané, že mikroorganizmy, ktoré kolonizujú pokožku, ovplyvňujú hojenie chronických rán, ktoré prevažujú v populácii vekovo staršej alebo majú cukrovku alebo obezitu. Úloha mikroorganizmov bola dobre študovaná v prípade diabetických vredov nôh (DVN). Odhaduje sa, že viac ako 50% DVN je infikovaných. DVN sú bežným výsledkom diabetes indukovanej neuropatie a vyskytujú sa u 15 až 25% jedincov s diabetom, pričom 15,6% si vyžaduje amputáciu. Z prieskumu 16S rRNA sa zistilo, že bakteriálne komunity, ktoré kolonizujú neuropatické DVN, boli spojené s klinickými príznakmi. Napríklad, plytké vredy s krátkym trvaním boli spojené s väčším počtom baktérií rodu Staphylococcus spp. Najmä S. aureus, zatiaľ čo hlbšie vredy s dlhším trvaním mali väčšiu mikrobiálnu rozmanitosť a vyššiu relatívnu abundanciu anaeróbnych baktérií a Gram-negatívnych proteobaktérií. Navyše, slabá kontrola glukózy v krvi bola spojená s väčším počtom baktérií rodu Staphylococcus spp. a Streptococcus spp.
Protirečivé výsledky
V longitudinálnom skríningu mikroorganizmov spojených s DVN sa sekvenovanie 16S rRNA rany ukázalo ako nestabilita bakteriálnej komunity, ktorá bola spojená s rýchlejším hojením rán a pozitívnejšími klinickými výsledkami. Toto pozorovanie je protirečivé, pretože mnohé štúdie na iných miestach tela odpozorovalo asociované choroby s nestabilitou bakteriálnej komunity. Avšak v kontexte rany môže mikrobiálna nestabilita viesť k účinnému odstráneniu baktérií z rany imunitným systémom. Okrem baktérií boli skúmané huby s amplifikáciou sekvencie ITS1 regiónu. Huby boli identifikované v 80% zo 100 analyzovaných DVN ako Cladosporium herbarum. Candida albicans bola identifikovaná ako najviac vyskytujúci sa druh. Pri chronických ranách so slabými klinickými prejavmi sa zvýšila diverzita húb a väčšinou sa našli polymikrobiálne biofilmy húb a baktérií spolu.
Závery
Stručne povedané, tieto zistenia poskytujú analýzu kožného mikrobiómu v oblasti zdravia a chorôb v doposiaľ nepreskúmanom rozlíšení. Analýza na tejto úrovni bola možná z dôvodu technického pokroku v metodikách extrakcie DNA a príprave sekvenčných knižníc, ktoré boli optimalizované pre rôznorodú, ale malú biomasu vzoriek kože. Navyše vývoj nových softvérových pomôcok, ktoré využívajú informácie do hĺbky, dispozícia metagenomických sekvenčných dát, rozšírilo naše chápanie ľudského kožného mikrobiómu. Mnohé otázky ako: akú úlohu majú mikroorganizmy v pokožke pri udržiavaní zdravia alebo pri podpore chorobných stavov? však zostávajú v súvislosti s funkciou kožného mikrobiómu nezopovedané.
DNA sekvenovanie je užitočným a nezaujatým nástrojom na odhaľovanie mikroorganizmov vo vzorkách, nie je však schopné rozlíšiť živé kolonizujúce mikroorganizmy od mŕtvych, prechodných organizmov. Hoci tradičné techniky založené na živých kultúrach dokážu rozlíšiť medzi živými a mŕtvymi mikroorganizmami, výsledky sú skreslené pretože veľa závisí od použitých podmienok kultivácie, a mnoho z nich je nekultivovatelných. Sekvencie RNA môžu riešiť tento problém odhalením funkčnej aktivity mikroflóry, ale tento postup je technicky náročný vzhľadom na nízku biomasu organizmov na koži. Pri nepriamom meraní tejto aktivity bola vyvinutá nová analytická metóda, ktorá porovnáva čítanie rozdelení na začiatku replikácie a tie, ktoré sa nachádzajú inde v genóme, ako dôkaz aktívnej bakteriálnej replikácie.
Analýza údajov o sekvenciách mikroorganizmov u pacientov v porovnaní so zdravými kontrolami sa môže použiť na vytvorenie hypotéz o údajných choroboplodných mikroorganizmoch. Záujmové organizmy sa potom môžu izolovať z jedincov prostredníctvom cielených metód kultivácie. Ďalej môžu tieto organizmy podstúpiť kompletné sekvenovanie genómu na analýzu ich funkčného potenciálu a môžu byť testované na zvieracích modeloch aby sa určili ich potenciálne mechanické funkcie v progresii ochorenia. Celkovo je cieľom preložiť údaje o sekvencii mikroorganizmov do funkčných štúdií, ktoré by mohli informovať o vývoji terapeutických modifikácií na zmiernenie dysbiózy a boj proti patogénom.
Použitá literatúra
Článok bol preložený z:
Allyson L. Byrd, Yasmine Belkaid, Julia A. Segre. 2018. The human skin microbiome. Nature Reviews Microbiology, volume16, pages143–155.
https://doi.org/10.1038/nrmicro.2017.157

Leave a Reply