Magdaléna Grófová, Lukáš Hleba
Slovenská poľnohospodárska univerzita v Nitre, Fakulta biotechnológie a potravinárstva, Ústav
Biotechnológie, Tr. Andreja hlinku 2, 949 76 Nitra.
Úvod
Ľudský mikrobióm predstavuje dynamický a funkčne významný biologický systém, ktorý zohráva kľúčovú úlohu v regulácii viacerých fyziologických procesov. Jeho formovanie sa začína bezprostredne po narodení a významne ovplyvňuje vývoj imunitného systému, metabolizmus aj dozrievanie nervovej sústavy.
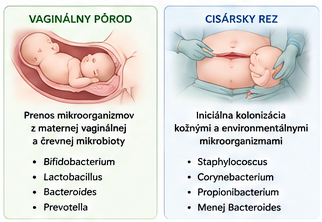
Zloženie mikrobiómu v ranom období života je determinované najmä spôsobom pôrodu a typom výživy. Pri vaginálnom pôrode dochádza k priamemu kontaktu novorodenca s maternálnou mikrobiotou, čo umožňuje efektívny prenos mikroorganizmov adaptovaných na ľudské črevné prostredie. Tento proces podporuje rýchlu iniciálnu kolonizáciu a následnú mikrobiálnu sukcesiu. Naopak, deti narodené cisárskym rezom sú primárne exponované kožným a environmentálnym mikroorganizmom, čo vedie k odlišnej trajektórii vývoja črevnej mikrobioty už v prvých dňoch života.
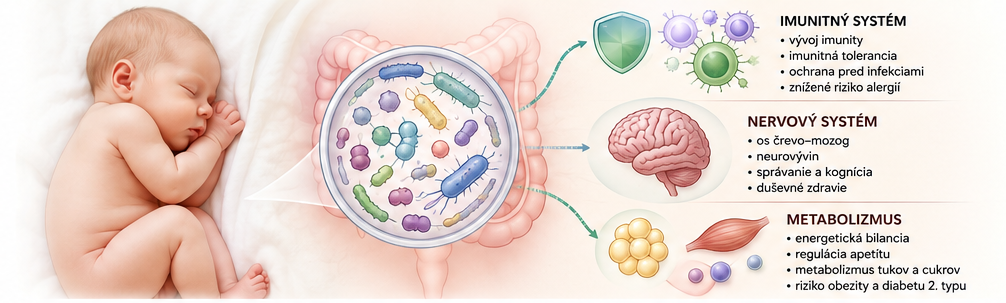
Významnú úlohu zohráva aj postnatálna výživa. Materské mlieko predstavuje komplexný biologický systém obsahujúci nielen živiny, ale aj mikroorganizmy, imunologicky aktívne molekuly a špecifické oligosacharidy, ktoré selektívne podporujú rast prospešných baktérií, najmä bifidobaktérií. Vďaka tomu prispieva k formovaniu mikrobioty s charakteristickým funkčným profilom. Naproti tomu dojčenská formula, napriek technologickému pokroku, vykazuje odlišné zloženie a jej vplyv na mikrobiálnu kolonizáciu vedie k rozdielom v diverzite aj metabolickej aktivite črevného mikrobiómu.
Raný postnatálny vývoj predstavuje kritické obdobie, počas ktorého sa formuje základná štruktúra a funkcia mikrobiálneho ekosystému. Tieto procesy majú potenciál ovplyvniť dlhodobé zdravie jedinca, vrátane imunitných, metabolických a neurovývinových aspektov. Pochopenie vzťahov medzi spôsobom pôrodu, výživou a vývojom mikrobiómu je preto kľúčové nielen z pohľadu základného výskumu, ale aj pre klinickú prax a preventívne stratégie.
Prvý kontakt s mikroorganizmami
Raný vývoj črevného mikrobiómu predstavuje dynamický proces, ktorý prebieha najmä počas prvých dní, týždňov a mesiacov života. V tomto období dochádza k postupnej mikrobiálnej sukcesii, pri ktorej sa jednotlivé bakteriálne skupiny striedajú v závislosti od podmienok v črevnom prostredí, dostupnosti substrátov a interakcií s hostiteľom.
Bezprostredne po narodení dominujú v čreve novorodenca najmä fakultatívne anaeróbne baktérie, ako sú zástupcovia rodu Enterobacteriaceae a Streptococcus. Tieto mikroorganizmy sú schopné prežívať v prítomnosti kyslíka a svojou metabolickou aktivitou postupne vytvárajú anaeróbne prostredie, ktoré umožňuje kolonizáciu striktne anaeróbnych baktérií. V nasledujúcej fáze preto dochádza k nárastu rodov Bifidobacterium, Bacteroides a ďalších anaeróbov, ktoré sa postupne stávajú dominantnou súčasťou črevnej mikrobioty.
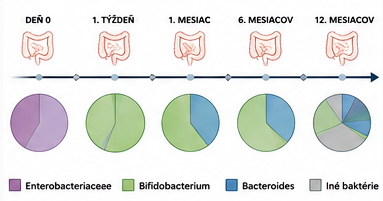
Spôsob pôrodu predstavuje jeden z hlavných determinantov tejto iniciálnej kolonizácie. Pri vaginálnom pôrode dochádza k priamemu kontaktu novorodenca s maternálnou mikrobiotou, čo podporuje rýchle osídlenie čreva baktériami adaptovanými na gastrointestinálne prostredie. Naopak, deti narodené cisárskym rezom sú primárne exponované kožným a environmentálnym mikroorganizmom, čo vedie k odlišnej trajektórii mikrobiálneho vývoja a často aj k nižšej počiatočnej diverzite.
Tieto rozdiely v skorom osídlení ovplyvňujú aj následnú mikrobiálnu sukcesiu v prvých týždňoch života. Mikrobiálny ekosystém je v tomto období charakteristický vysokou nestabilitou a citlivosťou na vonkajšie aj vnútorné faktory, vrátane výživy, kontaktu s matkou a expozície prostrediu. Postupne však dochádza k jeho stabilizácii a funkčnej diferenciácii.
Dôležitým aspektom je aj metabolická aktivita mikroorganizmov. Produkcia krátkoreťazcových mastných kyselín (SCFA), ako sú acetát, propionát a butyrát, zohráva kľúčovú úlohu v regulácii črevného prostredia, vývoji epitelovej bariéry a modulácii imunitnej odpovede. Tieto metabolity predstavujú významný spojovací článok medzi mikrobiómom a fyziológiou hostiteľa.
Významnú úlohu zohráva aj výživa novorodenca. Materské mlieko predstavuje komplexný biologický systém obsahujúci oligosacharidy, imunologicky aktívne molekuly a mikroorganizmy, ktoré selektívne podporujú rast prospešných baktérií, najmä bifidobaktérií. Výsledkom je charakteristický mikrobiálny profil s nižšou diverzitou, avšak vysokou funkčnou špecializáciou. Naopak, umelá mliečna výživa vedie k odlišnej mikrobiálnej dynamike, často spojenej s vyššou diverzitou a rozdielnym metabolickým profilom.
V priebehu prvých mesiacov života sa mikrobióm ďalej vyvíja a reaguje na zavádzanie pevnej stravy, ktoré predstavuje ďalší významný míľnik mikrobiálnej sukcesie. Tento proces vedie k zvýšeniu schopnosti degradácie komplexných polysacharidov a k postupnej stabilizácii mikrobiálneho ekosystému.
Z pohľadu vývojovej biológie ide o kritické „okno kolonizácie“, počas ktorého sa formuje základná štruktúra a funkcia črevného mikrobiómu. Hoci sa tento systém v priebehu detstva ďalej vyvíja a postupne približuje dospelému stavu, rané rozdiely v kolonizácii môžu zanechať dlhodobé funkčné dôsledky v metabolickom aj imunitnom nastavení organizmu.

Vplyv spôsobu pôrodu na mikrobióm
Spôsob pôrodu patrí medzi kľúčové faktory formujúce iniciálnu kolonizáciu črevného mikrobiómu a jeho ďalšiu vývojovú trajektóriu v ranom detstve. Rozdiely medzi vaginálnym pôrodom a cisárskym rezom sa neprejavujú len v počiatočnom zložení mikrobioty, ale aj v jej schopnosti stabilizácie, funkčnej adaptácie a mikrobiálnej maturácie.
Zásadnú úlohu zohráva mechanizmus prenosu mikroorganizmov z matky na dieťa. Pri vaginálnom pôrode dochádza k intenzívnemu vertikálnemu prenosu mikrobioty, pričom významným zdrojom nie je len vaginálne prostredie, ale aj črevná mikrobiota matky. Tento proces vedie k rýchlemu osídleniu čreva baktériami adaptovanými na intestinálne prostredie, najmä rodmi Bacteroides a Bifidobacterium, ktoré zohrávajú dôležitú úlohu v metabolizme komplexných sacharidov a v ranom programovaní imunitnej odpovede.
Pri cisárskom reze je tento prirodzený prenos výrazne obmedzený. Kolonizácia je v tomto prípade častejšie sprostredkovaná kožnými a environmentálnymi mikroorganizmami. Hoci sa môžu objaviť aj intestinálne baktérie, ich kolonizácia býva menej stabilná a niektoré kľúčové skupiny, ako napríklad Bacteroides, vykazujú tendenciu k postupnému útlmu. To naznačuje, že pre úspešné osídlenie čreva nie je rozhodujúca len expozícia mikroorganizmom, ale aj vhodné ekologické podmienky umožňujúce ich dlhodobé prežitie.
Tieto rozdiely sa odrážajú aj v dynamike mikrobiálnej stabilizácie. Mikrobiota detí narodených vaginálne vykazuje rýchlejšiu a konzistentnejšiu maturáciu, zatiaľ čo pri cisárskom reze je tento proces pomalší a variabilnejší. Výsledkom je odlišná časová trajektória vývoja, ktorá môže ovplyvniť funkčnú vyspelosť mikrobiálneho ekosystému v citlivom ranom období.
Rozdiely sa neprejavujú len na taxonomickej úrovni, ale aj vo funkčných vlastnostiach mikrobioty. Mikrobiálne spoločenstvá sa líšia v metabolickej aktivite, vrátane produkcie krátkoreťazcových mastných kyselín (SCFA), spracovania živín a interakcie s imunitným systémom hostiteľa. U detí narodených cisárskym rezom boli opísané odlišnosti v metabolických dráhach súvisiacich so sacharidovým a lipidovým metabolizmom, čo poukazuje na odlišné funkčné nastavenie mikrobiálneho ekosystému.
Je však dôležité zdôrazniť, že vplyv spôsobu pôrodu nepôsobí izolovane, ale je úzko prepojený s ďalšími faktormi, najmä s výživou. Dojčenie môže čiastočne zmierňovať rozdiely medzi deťmi narodenými vaginálne a cisárskym rezom a podporovať vývoj mikrobioty smerom k fyziologickejšiemu profilu. Naopak, umelá mliečna výživa môže tieto rozdiely udržiavať alebo prehlbovať, najmä v prípade absencie selektívnych substrátov podporujúcich rast prospešných baktérií.
Z dlhodobého hľadiska sa rozdiely medzi spôsobmi pôrodu postupne zmierňujú. Počas prvého roku života dochádza k čiastočnej konvergencii mikrobiálnych profilov, pričom významnú úlohu zohráva najmä výživa a expozícia prostrediu. Napriek tomu však rané odchýlky v kolonizácii môžu zanechať dlhodobejšie funkčné dôsledky v metabolickom a imunitnom nastavení organizmu.
Materské mlieko ako biologicky aktívny systém
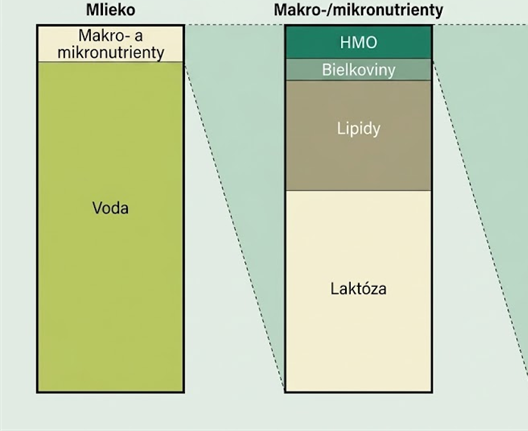
Materské mlieko nepredstavuje len zdroj energie a základných živín, ale komplexný biologický systém, ktorý aktívne ovplyvňuje vývoj novorodenca na viacerých úrovniach. Okrem makro- a mikronutrientov obsahuje široké spektrum bioaktívnych látok, ktoré sa podieľajú na formovaní črevného mikrobiómu, dozrievaní imunitného systému a fyziologickej adaptácii organizmu v ranom období života.
Jedným z kľúčových mechanizmov je modulácia mikrobiálnej kolonizácie čreva. Materské mlieko obsahuje vlastnú mikrobiotu, tvorenú najmä baktériami rodov Staphylococcus, Streptococcus, Lactobacillus a Bifidobacterium, ktoré sa môžu podieľať na osídlení gastrointestinálneho traktu novorodenca. Tento proces môže byť podporený aj tzv. entero-mamárnou osou, ktorá pravdepodobne umožňuje presun mikroorganizmov z čreva matky do mliečnej žľazy a následne k dieťaťu.
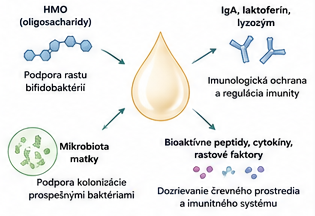
Zásadnú úlohu zohrávajú human milk oligosaccharides (HMO), ktoré patria medzi najvýznamnejšie funkčné zložky materského mlieka. HMO nie sú priamo využívané organizmom dieťaťa, ale slúžia ako selektívne substráty pre prospešné baktérie, najmä bifidobaktérie. Okrem toho pôsobia ako tzv. „decoy receptory“, ktoré inhibujú adherenciu patogénov na črevný epitel, čím prispievajú k ochrane organizmu. Týmto dvojitým mechanizmom významne formujú mikrobiálnu ekológiu čreva.
Materské mlieko má zároveň výraznú imunomodulačnú funkciu. Obsahuje široké spektrum imunologicky aktívnych molekúl vrátane sekrečného IgA, cytokínov, chemokínov a antimikrobiálnych proteínov, ako sú laktoferín a lyzozým. Sekrečný IgA zohráva kľúčovú úlohu v regulácii interakcií medzi mikroorganizmami a črevnou sliznicou, čím podporuje vznik imunologickej tolerancie a zároveň obmedzuje premnoženie potenciálne patogénnych baktérií.
Okrem klasických zložiek obsahuje materské mlieko aj ďalšie bioaktívne komponenty, ako sú rastové faktory, hormóny, mikroRNA, extracelulárne vezikuly a živé bunky vrátane imunitných buniek. Tieto prvky sa podieľajú na dozrievaní črevného epitelu, regulácii zápalových procesov a vývoji imunitnej rovnováhy. Ich účinok presahuje lokálne črevné prostredie a môže ovplyvňovať aj systémové procesy vrátane neurovývinu.
Dôležitou charakteristikou materského mlieka je jeho dynamické zloženie, ktoré sa mení v priebehu laktácie, počas dňa aj v rámci jednotlivých dávok. Táto adaptabilita umožňuje reagovať na meniace sa potreby dieťaťa a podporuje postupnú maturáciu mikrobiómu aj imunitného systému.
Z pohľadu vývoja črevného ekosystému tak materské mlieko nepredstavuje statický zdroj živín, ale komplexný regulačný systém, ktorý prostredníctvom viacerých paralelných mechanizmov formuje základnú biologickú trajektóriu raného života.
Umelá výživa (formula)
Dojčenská mliečna formula predstavuje dôležitú alternatívu výživy v situáciách, keď dojčenie nie je možné alebo je nedostatočné. Moderné formuly sú navrhnuté tak, aby sa čo najviac priblížili nutričnému zloženiu materského mlieka, avšak z hľadiska biologickej aktivity a vplyvu na črevný mikrobióm medzi nimi pretrvávajú významné rozdiely.
Jedným z kľúčových rozdielov je absencia živej mikrobioty a bunkových komponentov. Kým materské mlieko obsahuje široké spektrum mikroorganizmov, imunitných buniek a bioaktívnych molekúl, dojčenská formula je z mikrobiologického hľadiska sterilná. Aj keď sú do niektorých prípravkov pridávané probiotiká, ich kolonizačný potenciál a dlhodobá integrácia do črevného ekosystému sú limitované a nedosahujú úroveň prirodzeného vertikálneho prenosu.
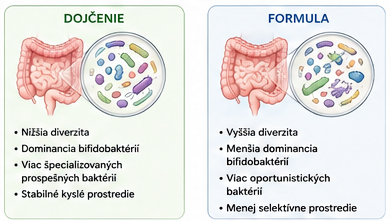
Tieto rozdiely sa odrážajú aj v zložení črevnej mikrobioty. U detí kŕmených formulou sa často pozoruje nižšie zastúpenie bifidobaktérií a vyšší podiel mikroorganizmov typických pre menej selektívne prostredie, vrátane rodov Clostridium alebo zástupcov čeľade Enterobacteriaceae. Mikrobiálne spoločenstvo je tak menej špecializované na využívanie substrátov charakteristických pre ľudské mlieko.
Významným faktorom je aj odlišné zastúpenie oligosacharidov. Materské mlieko obsahuje komplexnú zmes human milk oligosaccharides (HMO), ktoré selektívne podporujú rast prospešných baktérií. Tradičné formuly tieto štruktúry neobsahovali alebo len v obmedzenej miere. Hoci novšie generácie formulí obsahujú syntetické analógy HMO, ich diverzita a biologická funkčnosť zostávajú limitované v porovnaní s prirodzeným systémom.
Zaujímavým aspektom je vyššia mikrobiálna diverzita u detí kŕmených formulou v porovnaní s dojčenými deťmi. V ranom veku však vyššia diverzita nemusí nevyhnutne predstavovať výhodu, ale skôr odráža menej selektívne prostredie a nižšiu dominanciu funkčne špecializovaných baktérií. Z pohľadu vývoja ide preto o odlišnú organizačnú štruktúru mikrobiálneho ekosystému, nie o jeho vyššiu zrelosť.
Tieto rozdiely môžu mať aj dlhodobejšie dôsledky. Niektoré štúdie naznačujú asociácie medzi kŕmením formulou a zvýšeným rizikom alergických ochorení, obezity či metabolických porúch. Predpokladané mechanizmy zahŕňajú odlišnú imunitnú stimuláciu, zmenenú metabolickú signalizáciu a rozdiely v produkcii mikrobiálnych metabolitov.
V reakcii na tieto poznatky sa vývoj dojčenských formulí zameriava na ich funkčné obohacovanie. Do zloženia sa pridávajú probiotiká, prebiotiká, synbiotiká a postbiotiká, ako aj komplexnejšie oligosacharidové zmesi s cieľom priblížiť sa biologickým vlastnostiam materského mlieka. Napriek týmto snahám však zostáva formula funkčne odlišným systémom.
Osobitnú skupinu predstavuje kombinované kŕmenie, pri ktorom dieťa prijíma materské mlieko aj formulu. Mikrobióm má v tomto prípade prechodný charakter a jeho výsledný profil závisí od pomeru oboch zdrojov výživy. Aj čiastočný podiel materského mlieka však môže priaznivo ovplyvniť mikrobiálnu kolonizáciu a podporiť vývoj imunitného systému.
Kombinované kŕmenie
Kombinované kŕmenie, teda súčasné podávanie materského mlieka a dojčenskej formule, patrí v praxi medzi časté spôsoby výživy dojčiat. Z biologického hľadiska však nejde o jednoduchý prechod medzi dojčením a umelou výživou, ale o samostatný model, ktorý môže viesť k špecifickému vývoju črevného mikrobiómu.
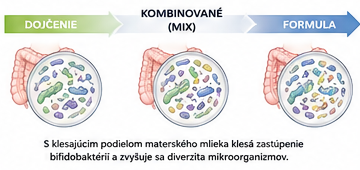
Dostupné poznatky naznačujú, že mikrobiálny profil kombinovane kŕmených detí sa líši od výlučne dojčených detí a v niektorých parametroch sa približuje skôr deťom kŕmeným formulou. Už v ranom období života možno pozorovať mikrobiálne aj metabolické charakteristiky, ktoré odrážajú vplyv oboch zdrojov výživy, pričom aj relatívne malý podiel formule môže ovplyvniť smerovanie mikrobiálneho vývoja.
Jedným z vysvetlení je narušenie selektívneho prostredia, ktoré vytvára materské mlieko. Pri výlučnom dojčení dochádza k podpore dominantného rastu bifidobaktérií, ktoré využívajú špecifické zložky mlieka, najmä oligosacharidy. Pridanie dojčenskej formule tento selektívny tlak oslabuje, čo vedie k širšiemu spektru kolonizujúcich mikroorganizmov a k nižšej dominancii funkčne špecializovaných bakteriálnych skupín.
Významnú úlohu zohráva aj pomer medzi materským mliekom a formulou. Kombinované kŕmenie predstavuje heterogénnu kategóriu, ktorá zahŕňa široké spektrum situácií – od minimálneho dokrmovania až po stav, keď formula tvorí dominantnú časť výživy. Hoci vyšší podiel materského mlieka spravidla podporuje mikrobiálny profil bližší dojčeným deťom, tento vzťah nie je striktne lineárny a môže byť modifikovaný ďalšími faktormi, ako sú spôsob pôrodu, expozícia antibiotikám či prostredie.
Z hľadiska vývoja mikrobiómu môže kombinované kŕmenie ovplyvniť aj časovanie mikrobiálnej maturácie. Prechod k stabilnej dominancii bifidobaktérií môže byť v porovnaní s výlučným dojčením oneskorený, čo naznačuje, že prítomnosť formule modifikuje prirodzenú trajektóriu kolonizácie čreva.
Na druhej strane kombinované kŕmenie zachováva časť biologických benefitov materského mlieka. Aj čiastočný príjem materského mlieka zabezpečuje prísun imunologicky aktívnych látok, ako sú imunoglobulíny, oligosacharidy a rastové faktory, ktoré prispievajú k modulácii črevného prostredia a podpore imunitného vývoja. Z tohto pohľadu preto nemožno kombinované kŕmenie považovať za ekvivalent výlučného kŕmenia formulou.
Dôležitým aspektom je aj interakcia medzi typom výživy a zavádzaním príkrmov. Mikrobióm detí kŕmených formulou alebo kombinovane vykazuje vyššiu citlivosť na zmeny v strave, zatiaľ čo materské mlieko môže pôsobiť stabilizačne a tlmiť vplyv nových dietárnych podnetov na mikrobiálnu komunitu.
Z klinického hľadiska je potrebné zdôrazniť, že kombinované kŕmenie je často determinované objektívnymi okolnosťami, ako sú obmedzená laktácia, zdravotný stav matky alebo sociálne faktory. Súčasné poznatky však naznačujú, že aj čiastočné dojčenie má biologický význam a môže priaznivo ovplyvniť vývoj črevného mikrobiómu v porovnaní s výlučným kŕmením formulou, hoci nedosahuje plný efekt exkluzívneho dojčenia.
Dlhodobé dôsledky raného mikrobiómu
Raný vývoj črevného mikrobiómu predstavuje obdobie, počas ktorého sa formujú základné interakcie medzi mikroorganizmami, imunitným systémom, metabolizmom a nervovou sústavou hostiteľa. Toto tzv. kritické „okno kolonizácie“ v prvých mesiacoch až rokoch života môže zásadne ovplyvniť dlhodobé zdravotné trajektórie jedinca, pričom niektoré jeho efekty sa prejavujú až v neskoršom detstve alebo v dospelosti.
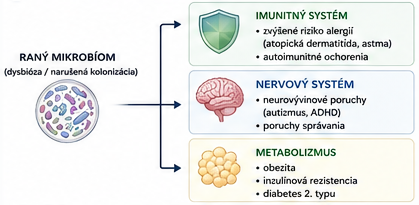
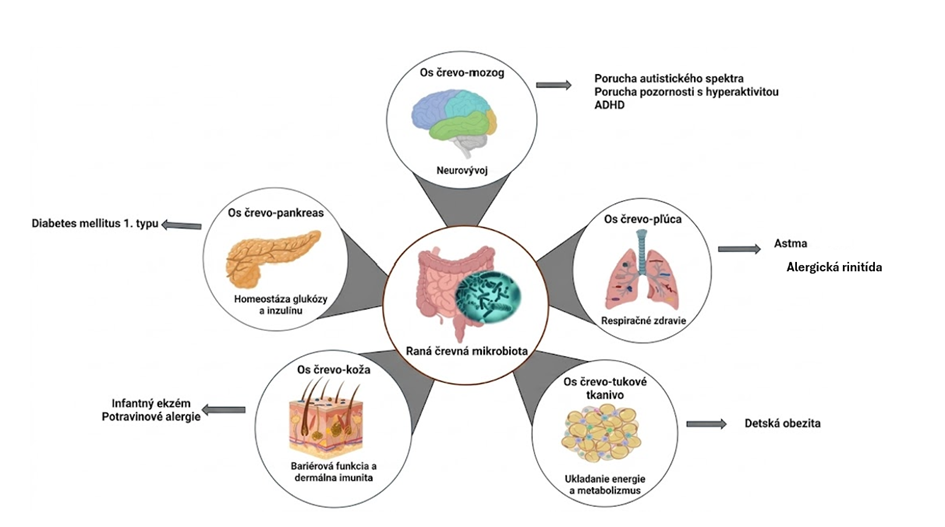
Jednou z najlepšie preskúmaných oblastí je vzťah medzi ranou mikrobiálnou kolonizáciou a vývojom imunitného systému. Fyziologické osídlenie čreva podporuje rovnováhu medzi imunitnou toleranciou a obrannými reakciami. Ak je tento proces narušený, napríklad v dôsledku odlišného spôsobu pôrodu alebo typu výživy, môže dochádzať k zvýšenej náchylnosti na alergické ochorenia, ako sú atopická dermatitída, potravinové alergie či astma. Predpokladané mechanizmy zahŕňajú zníženú stimuláciu regulačných T-lymfocytov a zmenenú produkciu krátkoreťazcových mastných kyselín (SCFA), ktoré zohrávajú dôležitú úlohu v protizápalovej regulácii a udržiavaní črevnej homeostázy.
Významnú úlohu zohráva aj os črevo–mozog, ktorá prepája črevný mikrobióm s vývojom centrálnej nervovej sústavy. Mikroorganizmy produkujú široké spektrum bioaktívnych metabolitov a signálnych molekúl, ktoré môžu ovplyvňovať neurovývinové procesy. Narušenie mikrobiálnej rovnováhy v ranom období bolo asociované so zvýšeným rizikom neurovývinových porúch, vrátane porúch autistického spektra, ADHD či behaviorálnych odchýlok. Tieto účinky sú pravdepodobne výsledkom komplexnej interakcie medzi imunitnou aktiváciou, metabolickou signalizáciou a vývojom neurálnych okruhov, pričom presné kauzálne mechanizmy zostávajú predmetom výskumu.
Raný mikrobióm sa podieľa aj na metabolickom programovaní organizmu. Zmeny v mikrobiálnej kolonizácii boli spojené so zvýšeným rizikom obezity, inzulínovej rezistencie a diabetu 2. typu. Predpokladá sa, že mikrobiota ovplyvňuje energetickú bilanciu hostiteľa prostredníctvom regulácie extrakcie energie zo stravy, modulácie apetítu a signalizačných dráh v tukovom tkanive.
Zásadnými determinantmi týchto procesov sú najmä spôsob pôrodu a výživa v ranom období života. Deti narodené vaginálne získavajú mikroorganizmy adaptované na črevné prostredie, zatiaľ čo pri cisárskom reze dominuje odlišný typ kolonizácie. Tento rozdiel je spojený s odlišnou trajektóriou vývoja mikrobioty, ktorá môže ovplyvniť imunitné aj metabolické nastavenie organizmu. Hoci sa rozdiely v mikrobiálnych profiloch postupne zmierňujú, ich funkčné dôsledky môžu pretrvávať.
Výživa predstavuje ďalší kľúčový faktor. Dojčené deti majú typicky mikrobióm dominovaný bifidobaktériami, ktoré podporujú imunitnú toleranciu a stabilitu črevného prostredia. Naopak, pri kŕmení formulou dochádza k odlišnej mikrobiálnej organizácii s vyššou diverzitou, ale nižšou dominanciou špecializovaných prospešných baktérií. Kombinované kŕmenie predstavuje intermediárny model, ktorého výsledný efekt závisí od pomeru jednotlivých zložiek výživy.
Z klinického hľadiska sa opakovane poukazuje aj na význam dĺžky dojčenia, pričom dlhšie obdobie exkluzívneho dojčenia je spojené s priaznivejším mikrobiálnym profilom a nižším rizikom niektorých ochorení v neskoršom veku. Raná mikrobiálna kolonizácia môže ovplyvňovať aj náchylnosť na infekčné ochorenia, čo poukazuje na jej význam v regulácii obranyschopnosti organizmu.
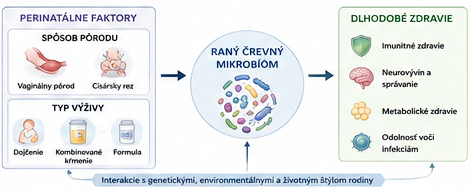
Napriek týmto poznatkom je potrebné interpretovať dostupné údaje s opatrnosťou. Väčšina štúdií má observačný charakter, a preto identifikované asociácie nemožno automaticky považovať za kauzálne vzťahy. Raný mikrobióm je ovplyvnený množstvom prepojených faktorov, vrátane genetických predispozícií, prostredia, antibiotickej expozície a životného štýlu, ktorých vzájomné interakcie môžu komplikovať interpretáciu výsledkov.
Ďalším limitom je metodologická heterogenita štúdií. Rozdiely v analytických prístupoch, časovaní odberov vzoriek a definíciách „zdravého mikrobiómu“ sťažujú porovnateľnosť výsledkov. Zároveň je potrebné zdôrazniť, že nie všetky rozdiely v mikrobiote sú patologické a časť variability predstavuje prirodzenú biologickú diverzitu.
Záver
Raný vývoj črevného mikrobiómu predstavuje kľúčový biologický proces, ktorý významne spoluutvára dlhodobý zdravotný stav človeka. Obdobie bezprostredne po narodení a prvé mesiace života predstavujú kritické „okno kolonizácie“, počas ktorého sa formuje základná štruktúra mikrobiálneho ekosystému a jeho prepojenie s imunitným, metabolickým a nervovým systémom.
Dostupné poznatky naznačujú, že charakter raného mikrobiómu je do značnej miery determinovaný perinatálnymi faktormi, najmä spôsobom pôrodu a typom výživy. Tieto premenné ovplyvňujú nielen iniciálnu kolonizáciu čreva, ale aj dynamiku jeho vývoja, stabilizáciu a funkčné nastavenie. Vaginálny pôrod je spojený s efektívnym prenosom maternálnych mikroorganizmov a rýchlejším etablovaním črevnej mikrobioty, zatiaľ čo cisársky rez vedie k odlišnej trajektórii jej vývoja. Podobne výživa predstavuje zásadný regulačný faktor, pričom materské mlieko podporuje selektívny rast prospešných baktérií a poskytuje komplexnú imunologickú a metabolickú signalizáciu, zatiaľ čo dojčenská formula vedie k odlišnej organizácii mikrobiálneho prostredia. Kombinované kŕmenie predstavuje intermediárny model, ktorého efekt závisí od pomeru jednotlivých zložiek výživy.
Z pohľadu dlhodobého zdravia sa rané rozdiely v mikrobiálnej kolonizácii spájajú so zmenenou náchylnosťou na viaceré ochorenia, vrátane alergických, metabolických a potenciálne aj neurovývinových porúch. Tieto súvislosti však nepredstavujú jednoduché kauzálne vzťahy, ale skôr výsledok komplexnej siete interakcií medzi mikrobiómom a hostiteľom.
Interpretácia dostupných poznatkov má zároveň svoje limity. Väčšina štúdií má observačný charakter a výsledky sú ovplyvnené viacerými prepojenými faktormi, ako sú genetická výbava, prostredie, antibiotická expozícia či socioekonomické podmienky. Metodologická heterogenita navyše komplikuje porovnateľnosť jednotlivých štúdií, čo si vyžaduje opatrný a kontextuálny prístup k interpretácii výsledkov.
Aj keď sú prirodzený pôrod a dojčenie často spájané s priaznivým vývojom mikrobiómu, v klinickej praxi ide o individuálne a často medicínsky podmienené rozhodnutia, ktoré nemožno hodnotiť jednostranne. Súčasný výskum však poukazuje na to, že mikrobióm predstavuje potenciálne modifikovateľný systém. Budúci vývoj v oblasti výživy, probiotických intervencií a personalizovanej medicíny môže umožniť cielene ovplyvňovať jeho zloženie a funkciu.
Pochopenie raných fáz mikrobiálnej kolonizácie tak otvára priestor pre nové preventívne stratégie zamerané na podporu zdravia už od začiatku života.
Zoznam použitej literatúry
Andreas, N. J., Kampmann, B., & Mehring Le-Doare, K. (2015). Human breast milk: A review on its composition and bioactivity. Early Human Development, 91(11), 629–635. https://doi.org/10.1016/j.earlhumdev.2015.08.013
Andres, S. F., Scottoline, B., & Good, M. (2023). Shaping infant development from the inside out: Bioactive factors in human milk. Seminars in Perinatology, 47(1), 151690. https://doi.org/10.1016/j.semperi.2022.151690
Bankole, T., & Li, Y. (2025). The early-life gut microbiome in common pediatric diseases: Roles and therapeutic implications. Frontiers in Nutrition, 12. https://doi.org/10.3389/fnut.2025.1597206
Borewicz, K., Suarez-Diez, M., Hechler, C., Beijers, R., de Weerth, C., Arts, I., Penders, J., Thijs, C., Nauta, A., Lindner, C., Van Leusen, E., Vaughan, E. E., & Smidt, H. (2019). The effect of prebiotic fortified infant formulas on microbiota composition and dynamics in early life. Scientific Reports, 9(1), 2434. https://doi.org/10.1038/s41598-018-38268-x
Borrego-Ruiz, A., & Borrego, J. J. (2025). Early-life gut microbiome development and its potential long-term impact on health outcomes. Microbiome Research Reports, 4(2), 20. https://doi.org/10.20517/mrr.2024.78
Boulangé, C. L., Pedersen, H. K., Martin, F.-P., Siegwald, L., Pallejà Caro, A., Eklund, A. C., Jia, W., Zhang, H., Berger, B., Sprenger, N., Heine, R. G., & CINNAMON Study Investigator Group. (2023). An extensively hydrolyzed formula supplemented with two human milk oligosaccharides modifies the fecal microbiome and metabolome in infants with cow’s milk protein allergy. International Journal of Molecular Sciences, 24(14), 11422. https://doi.org/10.3390/ijms241411422
Coker, M. O., Laue, H. E., Hoen, A. G., Hilliard, M., Dade, E., Li, Z., Palys, T., Morrison, H. G., Baker, E., Karagas, M. R., & Madan, J. C. (2021). Infant feeding alters the longitudinal impact of birth mode on the development of the gut microbiota in the first year of life. Frontiers in Microbiology, 12, 642197. https://doi.org/10.3389/fmicb.2021.642197
Chu, D. M., Ma, J., Prince, A. L., Antony, K. M., Seferovic, M. D., & Aagaard, K. M. (2017). Maturation of the infant microbiome community structure and function across multiple body sites and in relation to mode of delivery. Nature Medicine, 23(3), 314–326. https://doi.org/10.1038/nm.4272
Ferdous, T., Jiang, L., Dinu, I., Groizeleau, J., Kozyrskyj, A. L., Greenwood, C. M. T., & Arrieta, M.-C. (2022). The rise to power of the microbiome: Power and sample size calculation for microbiome studies. Mucosal Immunology, 15(6), 1060–1070. https://doi.org/10.1038/s41385-022-00548-1
Frias, J. P., Lee, M. L., Carter, M. M., Ebel, E. R., Lai, R.-H., Rikse, L., Washington, M. E., Sonnenburg, J. L., & Damman, C. J. (2023). A microbiome-targeting fibre-enriched nutritional formula is well tolerated and improves quality of life and haemoglobin A1c in type 2 diabetes: A randomized controlled trial. Diabetes, Obesity and Metabolism, 25(5), 1203–1212. https://doi.org/10.1111/dom.14967
Groer, M. W., Luciano, A. A., Dishaw, L. J., Ashmeade, T. L., Miller, E., & Gilbert, J. A. (2014). Development of the preterm infant gut microbiome: A research priority. Microbiome, 2(1), 38. https://doi.org/10.1186/2049-2618-2-38
Guo, C., Zhou, Q., Li, M., Zhou, L., Xu, L., Zhang, Y., Li, D., Wang, Y., Dai, W., Li, S., & Zhang, L. (2020). Breastfeeding restored the gut microbiota in caesarean section infants and lowered infection risk in early life. BMC Pediatrics, 20(1), 532. https://doi.org/10.1186/s12887-020-02433-x
Holst, A. Q., Myers, P., Rodríguez-García, P., Hermes, G. D. A., Melsaether, C., Baker, A., Jensen, S. R., & Parschat, K. (2023). Infant formula supplemented with five human milk oligosaccharides shifts the fecal microbiome closer to that of breastfed infants. Nutrients, 15(14), 3087. https://doi.org/10.3390/nu15143087
Jurgiel, J., Gromowski, T., Król, J., Bomba-Opoń, D., Kościółek, T., & Wielgoś, M. (2026). The impact of maternal microbial transfer on the infant gut microbiome after cesarean delivery: A systematic review. American Journal of Obstetrics and Gynecology, 233(6 Suppl), S541–S556. https://doi.org/10.1016/j.ajog.2025.09.001
Korpela, K. (2021). Impact of delivery mode on infant gut microbiota. Annals of Nutrition & Metabolism. https://doi.org/10.1159/000518498
Lazarini, T., Tonon, K. M., Araujo Filho, H. B., & Morais, M. B. (2025). Bifidogenic effect of 2′-fucosyllactose on the gut microbiome of healthy formula-fed infants. Nutrients, 17(6), 973. https://doi.org/10.3390/nu17060973
Le Doare, K., Holder, B., Bassett, A., & Pannaraj, P. S. (2018). Mother’s milk: A purposeful contribution to the development of the infant microbiota and immunity. Frontiers in Immunology, 9, 361. https://doi.org/10.3389/fimmu.2018.00361
Liu, Y., Ma, J., Zhu, B., Liu, F., Qin, S., Lv, N., Feng, Y., Wang, S., & Yang, H. (2023). Exclusive breastfeeding restores delivery mode-induced gut microbiota perturbations. Frontiers in Microbiology, 14, 1163269. https://doi.org/10.3389/fmicb.2023.1163269
Luo, D., Yang, L., Pang, H., Zhao, Y., Li, K., Rong, X., & Guo, J. (2022). Tianhuang formula reduces oxidative stress by regulating the gut microbiome. Frontiers in Microbiology, 13. https://doi.org/10.3389/fmicb.2022.984019
Madan, J. C., Hoen, A. G., Lundgren, S. N., Farzan, S. F., Cottingham, K. L., Morrison, H. G., Sogin, M. L., Li, H., Moore, J. H., & Karagas, M. R. (2016). Association of cesarean delivery and formula supplementation with the intestinal microbiome. JAMA Pediatrics, 170(3), 212–219. https://doi.org/10.1001/jamapediatrics.2015.3732
Mitchell, C. M., Mazzoni, C., Hogstrom, L., Bryant, A., Bergerat, A., Cher, A., Pochan, S., Herman, P., Carrigan, M., Sharp, K., Huttenhower, C., Lander, E. S., Vlamakis, H., Xavier, R. J., & Yassour, M. (2020). Delivery mode affects stability of early infant gut microbiota. Cell Reports Medicine, 1(9), 100156. https://doi.org/10.1016/j.xcrm.2020.100156
Myers, P. N., van Beijsterveldt, I. A. L. P., Snowden, S., Eriksen, C., Nielsen, H. B., Hughes, I. A., Ong, K. K., Hokken-Koelega, A., Koulman, A., & Brix, S. (2026). Breastfed infants receiving formula supplementation show altered lipid and gut microbiota profiles. Clinical Nutrition, 59, 106602. https://doi.org/10.1016/j.clnu.2026.106602
Naspolini, N. F., Schüroff, P. A., Vanzele, P. A. R., Pereira-Santos, D., Valim, T. A., Bonham, K. S., Fujita, A., Passos-Bueno, M. R., Beltrão-Braga, P. C. B., Carvalho, A. C. P. L. F., Klepac-Ceraj, V., Polanczyk, G. V., Campos, A. C., & Taddei, C. R. (2025). Exclusive breastfeeding is associated with gut microbiome maturation. Gut Microbes, 17(1), 2493900. https://doi.org/10.1080/19490976.2025.2493900
Perrett, B. M., Miliku, K., Moraes, T. J., Simons, E., Mandhane, P., & Kebbe, M. (2026). Gut microbiota responses to complementary food sources differ by milk feeding type. Clinical Nutrition, 58, 106587. https://doi.org/10.1016/j.clnu.2026.106587
Selma-Royo, M., Dubois, L., Manara, S., Armanini, F., Cabrera-Rubio, R., Valles-Colomer, M., González, S., Parra-Llorca, A., Escuriet, R., Bode, L., Martínez-Costa, C., Segata, N., & Collado, M. C. (2024). Birthmode and environment-dependent microbiota transmission dynamics are complemented by breastfeeding. Cell Host & Microbe, 32(6), 996–1010.e4. https://doi.org/10.1016/j.chom.2024.05.005
Stinson, L. F., Norrish, I., Mhembere, F., Cheema, A. S., Mullally, C. A., Payne, M. S., & Geddes, D. T. (2025). Seeding and feeding: Nutrition and birth-associated exposures shape gut microbiome assembly in infants. Gut Microbes, 17(1), 2557981. https://doi.org/10.1080/19490976.2025.2557981
van Best, N., Dominguez-Bello, M. G., Hornef, M. W., Jašarević, E., Korpela, K., & Lawley, T. D. (2022). Should we modulate the neonatal microbiome and what should be the goal? Microbiome, 10(1), 74. https://doi.org/10.1186/s40168-022-01281-4
Vatanen, T., Franzosa, E. A., Schwager, R., Tripathi, S., Arthur, T. D., Vehik, K., Lernmark, Å., Hagopian, W. A., Rewers, M. J., She, J.-X., Toppari, J., Ziegler, A.-G., Akolkar, B., Krischer, J. P., Stewart, C. J., Ajami, N. J., Petrosino, J. F., Gevers, D., Lähdesmäki, H., & Xavier, R. J. (2018). The human gut microbiome in early-onset type 1 diabetes. Nature, 562(7728), 589–594. https://doi.org/10.1038/s41586-018-0620-2
Vizzari, G., Morniroli, D., Ceroni, F., Verduci, E., Consales, A., Colombo, L., Cerasani, J., Mosca, F., & Giannì, M. L. (2021). Human milk: More than simple nourishment. Children, 8(10), 863. https://doi.org/10.3390/children8100863
Wang, M., Valizadegan, N., Fields, C. J., & Donovan, S. M. (2025). Fecal microbiome and metabolomic profiles of mixed-fed infants. Microorganisms, 13(1), 166. https://doi.org/10.3390/microorganisms13010166
Xu, D., & Wan, F. (2024). Breastfeeding and infant gut microbiota: Influence of bioactive components. Gut Microbes, 17(1), 2446403. https://doi.org/10.1080/19490976.2024.2446403
Zhao, L., Wang, S., Dong, J., Shi, J., Guan, J., Liu, D., Liu, F., Li, B., & Huo, G. (2021). Identification and antioxidant potential of Bifidobacterium longum strains. Frontiers in Microbiology, 12. https://doi.org/10.3389/fmicb.2021.756519
Zimmermann, P., & Curtis, N. (2020). Breast milk microbiota: Factors influencing composition. Journal of Infection, 81(1), 17–47. https://doi.org/10.1016/j.jinf.2020.01.023
Použité obrázky: Použité obrázky v článku sú generované AI (ChatGPT), alebo citované podľa aktuálne platných noriem.

Leave a Reply