
Maroš Lučaj, Lukáš Hleba
Slovenská poľnohospodárska univerzita v Nitre, Fakulta biotechnológie a potravinárstva
Úvod
Rakovina je identifikovaná nekontrolovaným množením abnormálnych buniek, ktoré majú za následok smrť človeka, keď nie sú kontrolované (obrázok č.1). Trvalo storočia, kým sme získali vedomosti a použili moderné technológie proti tejto chorobe. Považovaná je za nesmiernu globálnu záťaž, ktorá bude neustále priťahovať obrovskú spoločenskú pozornosť v dôsledku rastu a starnutia našej populácie. Správy prezentované Svetovou zdravotníckou organizáciou (WHO) informujú, že rakovina je druhou hlavnou príčinou úmrtí na celom svete. Počet prípadov sa zvyšuje každý rok a postihuje rôzne orgány ľudského tela. Súčasné výskumy sa zameriavajú na vývoj nových chemoterapeutických liekov získaných z prírodných aj syntetických zdrojov. Pomáha rozmanitosť prírodných zdrojov, ktorá ponúka obrovský potenciál pre objav nových zlúčenín s jedinečnými mechanizmami liečby rakoviny.
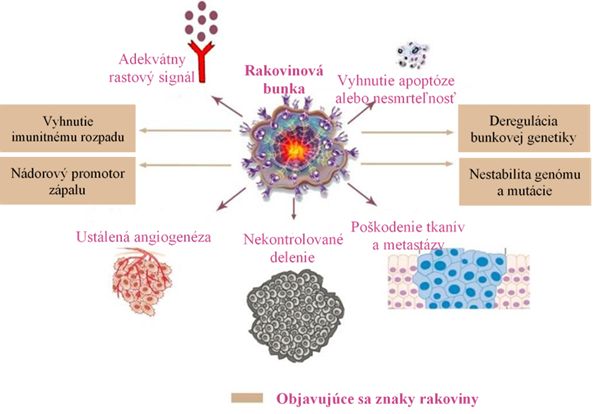
Všeobecné informácie
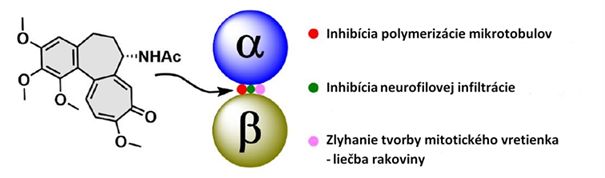
V priebehu histórie hrali prírodné produkty dominantnú úlohu pri liečbe ľudských chorôb. Napríklad objav penicilínu zmenil globálnu existenciu navždy. Taxány sú považované za jednu z najdôležitejších skupín chemoterapeutických látok proti rakovine. Najznámejším zástupcom je taxol, ktorý je povahou polyoxygenovaný diterpénový alkaloid s generickým názvom paklitaxel. Štruktúra je uvedená v obrázku č.2. Keď bolo schválené použitie taxolu ako protirakovinového lieku, tak jeho cena bola stanovená na 986 dolárov za dávku. Prognózy hovoria, že veľkosť globálneho trhu pre taxol ako lieku v období rokov 2020 až 2025 získajú rast s ročnou mierou rastu 8,2 %. Taxol je vysoko lipofilné liečivo a preto vykazuje veľmi zlú rozpustnosť (10–20 μM) vo vode. Pre pacientov sa použiva zmes kremoforu alebo etanolu, ktorá samotná môže vykazovať toxické účinky.
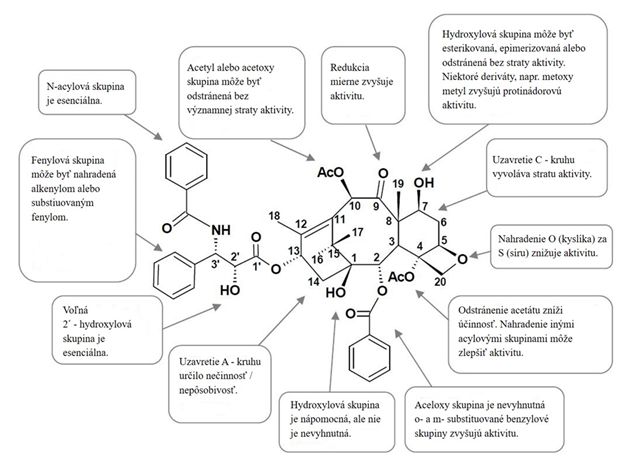
Klinická farmakológia taxolu v kocke
- Protinádorová aktivita: taxol ako liek je schválený na liečbu rakoviny vaječníkov, prsníka, pľúc a Kaposiho sarkómu súvisiaceho s HIV. Skúmal sa tiež pri liečbe (nemalobunkového karcinómu pľúc, malígneho melanómu, malígnych nádorov horných dýchacích ciest, akútnej leukémií, rakoviny močového mechúra, prostaty a pažeráka). Štúdie ukazujú, že taxol zvyšuje terapeutický pomer rádioterapie.
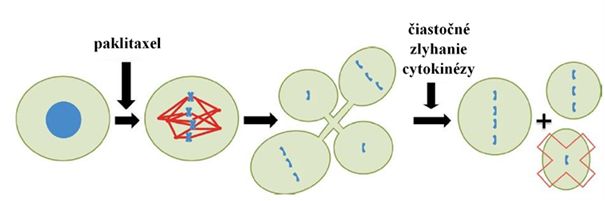
- Pri dávkovaní sa podáva ako 3-hodinová alebo 24-hodinová infúzia. Napríklad odporúčaná dávka na liečbu karcinómu vaječníkov a prsníka je 175 mg/m2 podávaných intravenózne počas 3 hodín každé 3 týždne. Menej ako 10 % dávky sa vylúči močom. Používa sa v liečbe s kombinácii s antracyklínmi. Individualizácia dávky na základe jedného merania plazmatickej koncentrácie 24 hodín po začiatku infúzie by mala byť schopná znížiť výskyt neutropénie. Rozdiel medzi kolchicínom (liek) a paclitaxelom je v tom, že kolchicín inhibuje zostavenie mikrotubulov, zatiaľ čo paclitaxel stabilizuje a chráni mikrotubuly pred rozložením. Paclitaxel potláča mikrotubuly s minimálnym odlúčením od centrozómov pri vyšších dávkach(obrázok č.7).
- Metabolizuje v pečeni a vylučuje sa žlčou. Taxol sa metabolizuje prostredníctvom cytochrómu P450.
Vedľajšie účinky
V súčasnosti klinicky veľa druhov rakoviny vykazuje dobrú odpoveď na konvenčné spôsoby liečby (chemoterapia a rádioterapia). Chemoterapia je primárnou možnosťou liečby pre najpokročilejších pacientov s rakovinou. Napriek intenzívnemu úsiliu zostáva toxicita a rezistencia na viaceré lieky dvoma hlavnými problémami, ktoré znižujú účinnosť liečby. Chemoterapia nepozná rozdiel medzi rakovinovými bunkami a normálnymi bunkami (obrázok č.3). Normálne bunky, ktoré sú najčastejšie ovplyvňované chemoterapiou, sú krvinky, bunky v ústach, žalúdku a črevách a vlasové folikuly. Taxol má interakcie s veľkým počtom liekov. Je známych celkovo 353 liekov, ktoré s ním interagujú. Pri použití taxolu a liekov (epirubicín, fosfenytoín, lapatinib, fenytoín, chinupristín) sa môže zvýšiť riziko vedľajších účinkov. Má tiež interakcie s tabakom a alkoholom. Prítomnosť zdravotných problémov (pomalá srdcová frekvencia, vysoký a nízky krvný tlak) môžu ovplyvňovať použitie tohto lieku v liečbe rakoviny. Za hlavný toxický účinok taxolu je považovaná neutropénia. Vyskytlo sa tiež niekoľko ďalších toxických účinkov (myalgie, mukozitída, reakcie z precitlivenosti a poruchy srdcového rytmu).
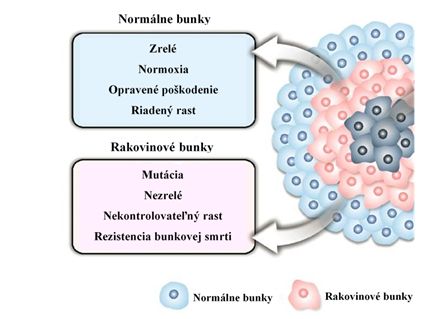
Zisk taxolu
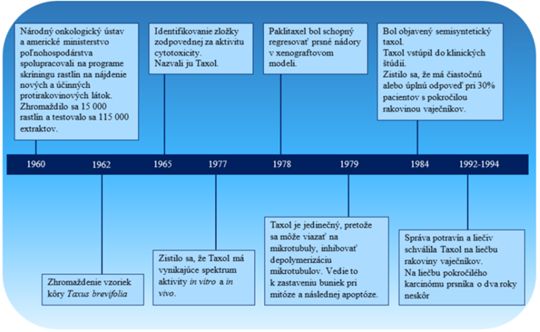
Štúdie o taxole sa uskutočňujú od okamihu jeho vývoja. Taxol je sekundárny metabolit tvorený každým druhom tisov v rôznych, ale malých množstvách. Taxol sa získava hlavne z rodu Taxus (čeľaďe Taxaceae). Do tohto rodu patria napríklad tieto druhy: Taxus brevifolia, Taxus chinensis, Taxus floridana, Taxus globosa, Taxus wallichiana, Taxus baccata, Taxus canadensis a Taxus cuspidata. Terapeutické vlastnosti tisu sa v praxi uplatňovali už v minulosti. Stopové množstvá taxolu sa našli aj v Cephalotaxus manii a Pseudotaxus chienii. Taxol našli aj v čeľadi Betulaceae. Obsah taxolu v týchto rastlinách bol však nižší ako v rastlinách Taxus. Taxol bol izolovaný z kôry stromu Taxus brevifolia (obrázok č.5), ktorý je známy ako tis západný alebo tis pacifický. V šesťdesiatych rokoch 20. storočia začalo testovanie rastlín z rodu Taxus (obrázok č.5). Spočiatku bol jediným zdrojom tejto zlúčeniny kôra Taxus brevifolia.. Celý postup izolácie zo surovej rastliny Taxus brevifolia bol ťažko namáhavý a s nízkym výťažkom. Izolácia 1 kg surového prírodného produktu si vyžiadala použitie 10 ton kôry tisu. To znamená, že by malo byť vyrúbaných 3000 stromov. Malo by sa tiež zdôrazniť, že 1 kg taxolu postačuje pre 500 pacientov. Taxus brevifolia je jedným z najpomalšie rastúcich stromov na svete. Bolo nevyhnutné vypracovať odlišné metódy zisku menej nákladnejšie a s vyšším výťažkom. V procese extrakcie sa získal z čerstvého ihličia Taxus baccata 10-deacetylbaccatín, ktorý bol štrukturálne blízky taxolu. Proces izolácie prešiel z priaznivejšieho materiálu a s vyšším výťažkom z 3 ton ihličia asi 1 kg látky. Postup navyše nevyžadoval ničenie tisov, pretože ihličie je ľahko obnoviteľné.Metódy získavania taxolu sa stále zlepšujú.

Zisk taxolu z endofytov
Na endofyty by sa malo pozerať ako na také mikroorganizmy, ktoré žijú v organelách rastlín bez toho, aby spôsobovali choroby. Toto tvrdenie sa všeobecne akceptuje. Formulácia hovorí, že endofyty sú mikroorganizmy, ktoré intercelulárne alebo intracelulárne kolonizujú a asymtomaticky infikujú rastlinné pletivá. Medzi mikroorganizmami a hostiteľom existujú interakcie na biochemickej a genetickej úrovni. Endofytické huby sú potenciálom pri produkcií nových bioaktívnych zlúčenin. Hodnotenie potenciálu niektorých endofytických húb spojených s rastlinami je perspektívne ako zdroj protirakovinových látok (tabuľka č.1). Taxol bol tiež izolovaný z endofytickej huby Taxomyces andreanae spojenej z kôry Taxus brevifolia a vykazoval protirakovinovú aktivitu.

Chemická syntéza paklitaxelu
Taxol je látka registrovaná ako terapeutické činidlo, pomenovaná ako paklitaxel. V roku 1994 bol úspešne syntetizovaný paklitaxel, ale mal zložitú molekulárnu štruktúru a jeho syntéza bola veľmi komplikovaná. Samotný proces zahŕňa celkovo 25-40 krokov. Komerčná výroba paklitaxelu navyše ešte nie je možná z hľadiska viacerých faktorov: kontrola reakčných podmienok, produkcia veľkého množstva toxických produktov a výrobné náklady, konečna cena produktu je extrémne vysoká.
Semisytéza paklitaxelu
Taxol je možné odvodiť semisyntézou analógov taxolu. Najdôležitejšie sú 10-deacetylbaccatin III, baccatin III a 10-deacetyltaxol. Semisyntéza začínajúca s prekurzorom taxolu, 10 deacetylbaccatinu III, ktorý je možné extrahovať z ihličia tisov. To sa ukázalo ako vhodná metóda. Okrem toho sa na semisyntézu taxolu môžu použiť aj ďalšie príbuzné taxány (baccatin III, cefalomanín, 10-deacetyl-7-xylosylpaklitaxel, 10-deacetyl-7-epipaklitaxel, 10-deacetyl-paklitaxel). Môže sa vyrábať vo veľkom množstve polosyntézou z baccatinu III z ihličia tisov. Produktivita sa zlepšila technikami semisyntézy, ale je to podobné so spotrebou tisov.
Biosyntéza paklitaxelu
Dráha biosyntézy paklitaxelu je rozdelená do troch krokov: 1. syntéza izopentenylpyrofosfátu (IPP) ako prekurzora terpénu, 2. syntéza Baccatinu III, 3. syntéza bočného reťazca. Ako prvé sa syntetizuje IPP a použije sa ako prekurzor pri biosyntéze paklitaxelu. Potom IPP generuje geranylgeranyl difosfát (GGPP) kondenzačnými reakciami a použitím geranylgeranyldifosfát syntázy (GGPPS). GGPP by mohol byť katalyzovaný prostredníctvom taxol-dién-cyklázy (TS) na to, aby sa cyklizoval na taxa-4(5)(12)-dién, ktorý sa považuje za krok obmedzujúci rýchlosť v syntéze. Baccatin III sa vyrába po hydroxylácii na uhlíku 1, C2, C5, C7, C9, C10 a C13. Vytvorí sa epoxypropánový kruh (C4 a C5), acylácia (C2, C5 a C10) a ketón (C9). Nakoniec bočný reťazec je syntetizovaný z fenylalanínu ako prekurzora. V tomto štádiu môže byť alfa-fenylalanín transformovaný na beta-fenylalanín, ktorý je následne možné previesť na fenylizoserín po hydroxylácii v mieste C2. Teraz fenylizoserín interaguje s hlavným reťazcom a vzniká zlúčenina paklitaxelu.
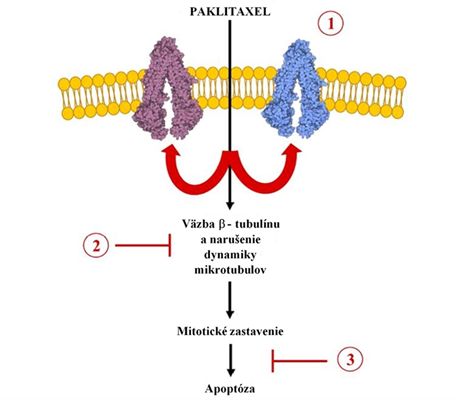
Mechanizmus účinku
Taxol/paklitaxel je známy ako činidlo zacielujúce na mikrotubuly (MTAs). Mikrotubuly sú rezistentné na depolymerizáciu vápnikom a studeným podmienkami, ktoré depolymerizujú normálne mikrotubuly. Mikrotubuly majú v eukaryotických bunkách funkcie, kedy sa podieľajú na mitóze, udržiavaní bunkového tvaru, motilite a intracelulárnom prenose organel a makromolekúl. Na účasť na týchto činnostiach musia byť mikrotubuly vysoko dynamické. Taxol je schopný inhibovať dynamiku mikrotubulov. Mechanizmus účinku spočíva v stabilizácii mikrotubulov v bunke, ktoré pôsobia proti ich depolimerizácii. Proces inhibuje správne oddelenie dvoch identických súborov chromozómov a ich prenos počas delenia buniek. Ďalej spôsobuje blokovanie bunkovej mitózy a následne indukuje bunkovú smrť. Taxol vďaka svojmu hydrofóbnemu charakteru ľahko prechádza plazmatickou membránou. Keď je v cytoplazme, viaže sa s vysokou afinitou na podjednotku tubulínu a modifikuje stabilizuje mikrotubuly. Taxol sa tiež viaže na BCL-2 proteín zapojený do procesu apoptózy. Bunkové účinky taxolu sa líšia v závislosti od dávky. V rozsahu nanomolárnych koncentrácií indukuje trvalé mitotické zastavenie, inhibuje prenyláciu proteínov a spúšťa apoptózu. V mikromolárnych dávkach podporuje syntézu a uvoľňovanie cytokínov, ako je tumor nekrotizujúci faktor (TNF) a interleukíny (IL1 a IL8), zvyšuje fosforyláciu tyrozínu kinázami a stimuluje produkciu oxidu dusnatého.
Imunoterapia nádorov
Paklitaxel/taxol priamo zabíja nádorové bunky a reguluje rôzne imunitné bunky (efektorové T bunky, dendritické bunky, NK bunky, regulačné T bunky a makrofágy). Imunoterapia nádorov funguje prostredníctvom niekoľkých mechanizmov: podporou proliferácie a aktivácie T buniek, zvýšením aktivity B-buniek a zvýšením produkcie protilátok, zvýšením počtu NK buniek výrobou účinných látok a zlepšením krvotvorby tela.
· nadmerná expresia transmembránových efluxných transportérov (ABCB1, ABCC10),
· mutácie tubulínu (alfa a beta) alebo zmeny stability siete mikrotubulov,
· znížená funkcia významných apoptotických proteínov ( Bcl-2 a p53).
Upravené podľa (Barbuti a Chen, 2015).
Záver
Očakáva sa, že pomer pacientov s rakovinou sa do roku 2040 globálne zvýši až na 27,5 milióna. Neustále prebieha vývoj prírodných liečivých zlúčenín, ktoré sa testujú na klinické použitie pri liečbe, aby sa nahradila rádioterapia a chemoterapia a znížili sa ich vedľajšie účinky. Takže boj nikdy nekončí. Taxol/paklitaxel bol podaný viac ako miliónu pacientov s rakovinou a preukázal nádej pri liečbe neurodegeneratívnych chorôb. Ukázal sa ako nenahraditeľný prostriedok pri štúdiu v bunkovej biológii, kde sa zameriava na úlohu systému tubulín/mikrotubuly (obrázok č.8). Metabolické inžinierstvo a syntetická biológia ponúkajú potenciál ideálneho prírodného alebo syntetického základu pre syntézu sekundárneho metabolitu taxolu do budúcnosti. Produkcia zo vzťahu rastlina a endofytické huby má potenciál do budúcich výskumov, ako aj výskum v biosyntetickej dráhe taxolu.
Zoznam použitej literatúry
ADELEKE, Bartholomew Saanu – BABALOLA, Olubukola Oluranti. 2021. Pharmacological Potential of Fungal Endophytes Associated with Medicinal Plants: A Review. In Journal of Fungi [online], vol. 7, no. 2, pp. 147-163 [cit. 2021-01-05]. https://doi.org/10.3390/jof7020147
AGLAWE, Sachin – GAYKE, Amol – KADAM, Pratik – KANAWADE, Shubham – GARUD, Yogesh. 2019. TAXOL AS AN ANTICANCER AGENT: A REVIEW. In Int. J. Res. Ayurveda Pharm. [online], vol. 10, no. 6, pp. 15-17 [cit. 2021-03-15]. https://doi.org/10.7897/2277-4343.1006116
ARONSON, J.K. 2016. Meyler’s Side Effects of Drugs The International Encyclopedia of Adverse Drug Reactions and Interactions 16 Edition. Elsevier Science, pp. 445-452. ISBN 978-0-444-53716-4.
BARBUTI, Anna Maria – CHEN, Zhe-Sheng. 2015. Paclitaxel Through the Ages of Anticancer Therapy: Exploring Its Role in Chemoresistance and Radiation Therapy. In Cancers [online], vol. 7, no. 4, pp. 2360-2371 [cit. 2020-03-20]. https://doi.org/10.3390/cancers7040897
BHAT, Mohammad Aamir – VARSHNEYA, Chandresh – BHARDWAY, Pallavi – PATIL, Rajendra Damu. 2016. Paclitaxel – Development, Properties, Toxicity/Safety Evaluation and the Scope of Improvement. In IOSR Journal of Biotechnology and Biochemistry [online], vol. 2, no. 4, pp. 40-48, ISSN: 2455-264X [cit. 2020-03-20]. https://www.researchgate.net/publication/342976959_Paclitaxel_-Development_Properties_ToxicitySafety_Evaluation_and_the_Scope_of_Improvement
CRAGG, Gordon M. – PEZZUTO, John M. 2015. Natural Products as a Vital Source for the Discovery of Cancer Chemotherapeutic and Chemopreventive Agents. In Med Princ Pract. [online], vol. 25, no. 2, pp. 41–59 [cit. 2020-03-10]. https://doi.org/10.1159/000443404
DESHMUKH, Sunil K. – GUPTA, Manish K. – PRAKASH, Ved – REDDY, Sudhakara M. 2018. Mangrove-associated fungi: a novel source of potential anticancer compounds. In Journal of Fungi [online], vol. 4, no. 3, pp. 101 [cit. 2021-03-10]. https://doi.org/10.3390/jof4030101
FADIJI, Ayomide Emmanuel – BABALOLA, Olubukola Oluranti. 2020. Elucidating Mechanisms of Endophytes Used in Plant Protection and Other Bioactivities With Multifunctional Prospects. In Front Bioeng Biotechnol. [online], vol. 8, no. 467, pp. 1-20 [cit. 2021-05-01]. https://doi.org/10.3389/fbioe.2020.00467
GALLERO-JARA, Julia – LOZANO-TEROL, Gema – SOLA-MARTINEZ, Rosa Alba – CANOVAS-DIAZ, Manuel – DE DIEGO-PUENTE, Teresa. 2020. A Compressive Review about Taxol®: History and Future Challenges. In Molecules [online], vol. 25, no. 24, pp. 5986-6010 [cit. 2021-04-15]. https://doi.org/10.3390/molecules25245986
GEORGATOS, Spyros – D. THEODOROPOULOS, Panayiotis A. 2011. Taxol. In Schwab, Manfred. Encyclopedia of Cancer. Berlín : Springer, pp. 1-3. ISBN 978-3-642-16484-2. https://doi.org/10.1007/978-3-642-27841-9_5690-2
GLISIC, Sanja – VELJKOVIC, Veljko. 2018. Design of targeting peptides for nanodrugs for treatment of infectious diseases and cancer. In Grumezescu, Alexandru Mihai. Drug Targeting and Stimuli Sensitive Drug Delivery Systems. William Andrew, pp. 343-381. ISBN 978-0-12-813689-8.
HAN, Jiyou – WON, Miae – KIM, Ji Hyeon – JUNG, Eugeine – MIN, Kyungim – JANGILIB, Paramesh KIM, Jong Seung. 2020. Cancer stem cell-targeted bio-imaging and chemotherapeutic perspective. In Chem. Soc. Rev. [online], vol. 49, no. 22, pp. 7856-7878 [cit. 2021-03-10]. https://doi.org/10.1039/d0cs00379d
HAYEE, Sara – REHMAN, Amna Rehman. 2012. Cancer: A Life Threatening Peril Becoming Lifestyle Disease. In Pakistan Journal of Physical Therapy [online], vol. 3, no. 3, ISSN: 2663-080X [cit. 2021-03-12]. https://doi.org/10.52229/pjpt.v3i3.902
HEMPEL, Georg. 2020. Dose and therapy individualization in cancer chemotherapy. In Handbook of Analytical Separations. vol. 7, pp. 291- 319. https://doi.org/10.1016/b978-0-444-64066-6.00013-7
KAMPAN, Nirmala Ch. – MADONDO, Mutsa T. – MCNALLY, Orla M. – QUINN, Michael – PLEBANSKI, Magdalena. 2015. Paclitaxel and its evolving role in the management of ovarian cancer. In BioMed Research International [online], vol. 2015, no. 413076 [cit. 2020-03-10]. https://doi.org/10.1155/2015/413076
LIU, W. C. – GONDA, T. – ZHU, P. 2016. Advances in exploring alternative Taxol sources. In RSC Advances [online], vol. 6, no. 54, pp. 48800-48809 [cit. 2020-04-08]. https://doi.org/10.1039/c6ra06640b
MAMADALIEVA, N. Z. – MAMEDOV, N. A. 2020. Taxus brevifolia a High-Value Medicinal Plant, as a Source of Taxol. In Máthé, Ákos. Medicinal and Aromatic Plants of North America. Chan : Springer, pp. 201-218. ISBN 978-3-030-44928-5.
MCELROY, Christopher – JENNEWEIN, Stefan. 2017. Taxol® Biosynthesis and Production: From Forests to Fermenters. In Schwab, Wilfried – Lange, Bernd Markus – Wüst, Matthias. Biotechnology of Natural Products. Cham : Springer, pp. 145-185. ISBN 978-3-319-67903-7.
MENDOZA, Nadia – SILVA, Eleazar M. Escamilla. 2018. Introduction to Phytochemicals: Secondary Metabolites from Plants with Active Principles for Pharmacological Importance. In Asao,Toshiki – Asaduzzaman, Md. Phytochemicals – Source of Antioxidants and Role in Disease Prevention. Intechopen, pp.26-46. ISBN: 978-1-83881-711-4.
MIYOSHI, Norikatsu – HARAGUCHI, Naotsugu – MIZUSHIMA, Tsunekazu . ISCHII, Hideshi – YAMAMOTO, Hirofumi – MORI, Masaki. 2021. Targeting cancer stem cells in refractory cancer. In Regenerative Therapy [online], vol. 17, pp. 13-19 [cit. 2021-04-12]. https://doi.org/10.1016/j.reth.2021.01.002
NAVEED, Muhammad – RAEES, Mohammad – LIAQAT, Irfan – KASHI, Mohammad. 2018. Clastogenic ROS and biophotonics in precancerous diagnosis. In Front. Biol. [online], vol. 13, pp. 103–122 [cit. 2020-03-19]. https://doi.org/10.1007/s11515-018-1488-0
PETRINI, Orlando. 1991. Fungal endophytes of tree leaves. In Andrews John H. – Hirano Susan S. Microbial ecology of leaves. New York : Springer, pp. 179-197. ISBN 978-1-4612-3168-4.
SABZEHZARI, Mohammad – ZEINALI, Masoumeh – NAGHAVI, Mohammad Reza. 2020. Alternative Sources and Metabolic Engineering of Taxol: Advances and Future Perspectives. In Biotechnology Advances [online], vol. 43, pp. 1-35 [cit. 2020-05-01]. https://doi.org/10.1016/j.biotechadv.2020.107569
SINGH, Khusbu – DWIVEDI, Gaurav Raj – SANKET, A. – PATI, Sanghamitra. 2019. Therapeutic Potential of Endophytic Compounds: A Special Reference to Drug Transporter Inhibitors. In Current Topics in Medicinal Chemistry [online], vol. 19, pp. 1-28 [cit. 2020-04-20]. https://doi.org/10.2174/1568026619666190412095105
SINHA, Dwaipayan. 2020. A REVIEW ON TAXANES: AN IMPORTANT GROUP OF ANTICANCER COMPOUND OBTAINED FROM TAXUS SP. In International Journal of Pharmaceutical Sciences and Research [online], vol. 11, no. 5, pp. 1969-1985 [cit. 2021-04-20]. ISSN: 0975-8232. https://doi.org/10.13040/ijpsr.0975-8232.11(5).1969-85
ŠKUBNIK, Jan – JURAŠEK, Michal – RUML, Tomáš – RIMPELOVA, Silvie. 2020. Mitotic Poisons in Research and Medicine. In Molecules [online], vol. 25, no. 20, pp. 4632-4673 [cit. 2020-05-01]. https://doi.org/10.3390/molecules25204632
VARSHA, Kumari Varsha – SHARMA, Ankita – KAUR, Amanpreet – MADAN, Jitender – PANDEY, Ravi S. – JAIN, Upendra K. – CHANDRA, Ramesh. 2017. Natural plant-derived anticancer drugs nanotherapeutics: a review on preclinical to clinical success. In Ficai, Anton – Grumezescu, Alexandru Mihai. Nanostructures for Cancer Therapy. Bucharest : Elsevier, pp. 776-799. ISBN 978-0-323-46144-3.
WEAVER, Beth A. 2014. How Taxol/paclitaxel kills cancer cells. In Molecular Biology of the Cell [online], vol. 25, no. 18, pp. 2677–2681 [cit. 2021-04-20]. https://doi.org/10.1091/mbc.e14-04-0916
WILSON, Dennis. 1995. Endophyte: The Evolution of a Term, and Clarification of Its Use and Definition. In Nordic Society Oikos [online], vol. 73, no. 2, pp. 274–276 [cit. 2021-04-17]. https://doi.org/10.2307/3545919
YANG-HUANG, Chia-Ping – HORWITZ-BAND, Susan. 2017. Taxol®: The First Microtubule Stabilizing Agent. In International Journal o f Molecular Sciences [online], vol. 18, no. 8, pp. 1733-1744 [cit. 2020-04-17]. https://doi.org/10.3390/ijms18081733
ZHANG, Hui – QIU, Longhui. 2019. Bruton’s Tyrosine Kinase (BTK) Inhibitors as Sensitizing Agents for Cancer Chemotherapy. In CHEN, Zhe-Sheng Chen – YANG, Dong-Hua. Protein Kinase Inhibitors as Sensitizing Agents for Chemotherapy. USA : Academic Press, 256 s. ISBN 978-0-12-816435-8.
ZHU, Linyan – CHEN, Liqun. 2019. Progress in research on paclitaxel and tumor immunotherapy. In Cellular & Molecular Biology Letters [online], vol. 24, no. 40, pp. 1-11 [cit. 2021-04-21]. Dostupné na: DOI: 10.1186/s11658-019-0164-y. ZWAWIAK, Justyna – ZAPRUTKO, Lucjusz. 2014. A brief history of taxol. In Journal of Medical Science[online], vol. 1, no. 83, pp. 47-53 [cit. 2021-04-20]. https://www.researchgate.net/publication/267035097_A_brief_history_of_taxol

Leave a Reply